Questões de Química - Sistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum. para Concurso
Foram encontradas 14 questões
Observe a tabela a seguir que contém os valores de pKa para cinco ácidos inorgânicos distintos.
ÁCIDO pKa carbônico 6,37 hipocloroso 7,53 hipobromoso 8,69 bórico 9,14 cianídrico 9,31
O ácido mais forte é o
A tabela a seguir contém os valores das constantes de equilíbrio de alguns ácidos e bases.
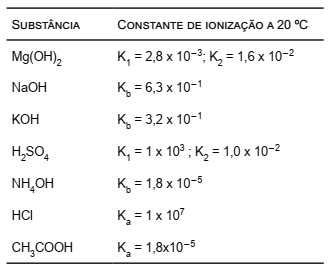
Uma das reações de identificação dos íons magnésio consiste em precipitá-lo com base forte, formando o hidróxido de magnésio, branco, segundo a equação:
Mg2+ (aq) + 2OH–(aq)  Mg(OH)2
(s)
Mg(OH)2
(s)
O precipitado formado pode ser dissolvido quando ao
meio aquoso é adicionado o sal


Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H2O2 igual a 2,4 × 10-12, julgue o item a seguir.
Em solução aquosa com pH igual a 10,0, o grau de ionização
ácida do H2O2 é superior a 2,0%.
O equilíbrio de dissociação da água é mostrado na equação de equilíbrio a seguir:
H2O ⇋ H+ + OH-
A 25°C, a constante de equilíbrio (Kw) é dada por:
Kw = [H+] [OH- ] = 1,0 x 10-14
Ao se misturarem 50 mL de uma solução aquosa do ácido
forte HCℓ (0,01 mol L-1
) com 20 mL de solução aquosa da
base forte KOH (0,02 mol L-1
) e água suficiente para se
levar o volume final a 100 mL, o pH da solução resultante,
a 25°C, será