Questões de Física - Gás Ideal para Concurso
Foram encontradas 75 questões
Q2364549
Física
Considere uma situação hipotética envolvendo 25 mols de um gás ideal monoatômico
que passa por um processo reversível de expansão isobárica. O gás inicialmente está a uma
temperatura de 150 K e ocupa um volume de 2 m3. Durante esse processo, a temperatura cai para
100 K e o volume aumenta para 3 m3. Admitindo que esse gás apresenta um calor específico molar a
volume constante de 4,1 J/molK, qual é, aproximadamente, a variação de entropia desse gás para
essa situação hipotética? Considere R = 8,31 j/molK In 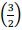 = 0,41 e In
= 0,41 e In 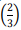 = −0.41.
= −0.41.
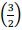 = 0,41 e In
= 0,41 e In 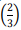 = −0.41.
= −0.41.
Q2364544
Física
Considere um balão meteorológico, constituído de um filme plástico expansível e
preenchido com hidrogênio, que se comporta de maneira aproximada a um gás ideal, deslocando-se
verticalmente na atmosfera devido exclusivamente às forças de empuxo e peso. Suponha que o balão
seja liberado do nível do mar, em um dia cuja temperatura ambiente é de 27°C, com um raio
aproximado de 1,5 m. À medida que o balão sobe até uma altitude de 45 km, onde a temperatura
ambiente diminui em 40°C, a pressão no interior do balão reduz-se a 1/10 da pressão inicial. Nessas
condições, o raio aproximado do balão, ao atingir a altitude máxima descrita, será de:
Ano: 2023
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2023 - Transpetro - Profissional Transpetro de Nível Superior - Junior: Ênfase 9: Comercialização e Logística - Transporte Marítimo |
Q2326213
Física
A equação de Clapeyron para um gás ideal estabelece
a relação da temperatura absoluta (T), da pressão (ρ) e
do volume (V) desse gás com o número de moles (n) e
a constante universal dos gases ideais (R). Admita que,
após uma determinada transformação de um gás ideal de
massa constante, sua pressão e seu volume duplicaram.
Nesse caso, a temperatura do gás, em grau Kelvin,
Nesse caso, a temperatura do gás, em grau Kelvin,
Q2297518
Física
A partir da teoria cinética, tem-se que as moléculas de um gás mantêm um movimento aleatório e podem
sofrer colisões. Entre duas colisões sucessivas, uma molécula se move em linha reta com velocidade
uniforme. Tal percurso entre duas colisões sucessivas é chamado de Livre Caminho Médio e pode ser
expresso pela equação:
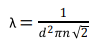
onde λ é o livre caminho médio; d é o diâmetro da molécula; n é a densidade das moléculas no meio (moléculas/m3 ).
Considere uma amostra de oxigênio a 27 ºC e 1 atm (101,3×103 Pa). Calcule o livre caminho médio da molécula de oxigênio, considerando o sistema como um gás ideal e que o tamanho da molécula de oxigênio é de 2,9 Å.
Dados: Constante de Boltzmann k = 1,381×10-23 J.K-1.
O valor calculado é, aproximadamente,
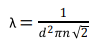
onde λ é o livre caminho médio; d é o diâmetro da molécula; n é a densidade das moléculas no meio (moléculas/m3 ).
Considere uma amostra de oxigênio a 27 ºC e 1 atm (101,3×103 Pa). Calcule o livre caminho médio da molécula de oxigênio, considerando o sistema como um gás ideal e que o tamanho da molécula de oxigênio é de 2,9 Å.
Dados: Constante de Boltzmann k = 1,381×10-23 J.K-1.
O valor calculado é, aproximadamente,
Q2297500
Física
A figura 1 mostra esquematicamente a variação da pressão com o volume para um gás real em várias
temperaturas, sendo T1 > T2 > T3 > T4 > T5.
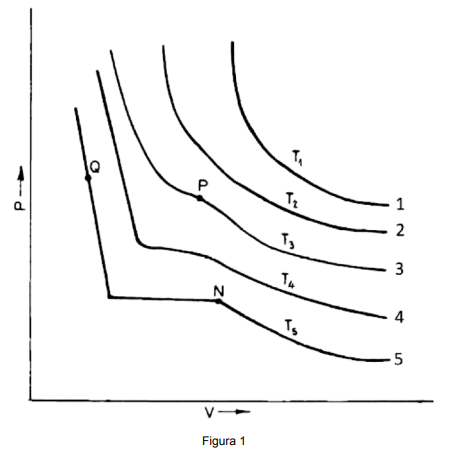
Assinale V (verdadeiro) ou F (falso) diante de cada afirmativa a seguir.
( ) As curvas 1 e 2 seguem a Lei de Boyle para um gás ideal.
( ) O ponto P é conhecido como Ponto Triplo
( ) O ponto N é chamado de Ponto Crítico.
( ) O material no ponto Q está em estado líquido.
Assinale a alternativa com a sequência correta.

Assinale V (verdadeiro) ou F (falso) diante de cada afirmativa a seguir.
( ) As curvas 1 e 2 seguem a Lei de Boyle para um gás ideal.
( ) O ponto P é conhecido como Ponto Triplo
( ) O ponto N é chamado de Ponto Crítico.
( ) O material no ponto Q está em estado líquido.
Assinale a alternativa com a sequência correta.