Questões da Prova Exército - 2011 - EsPCEx - Cadete do Exército - 3° Dia
Foram encontradas 40 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Dados: Kw = 10-14 (mol · L-1)2
Em uma tabela, são dados 4(quatro) compostos orgânicos, representados pelos algarismos 1,2,3 e 4, e seus respectivos pontos de ebulição, à pressão de 1 atm. Esses compostos são propan-1-ol, ácido etanóico, butano e metoxietano, não necessariamente nessa ordem.
Sobre os compostos e a tabela acima são feitas as seguintes afirmações:
I- Os compostos 1, 2, 3 e 4 são respectivamente butano, metoxietano, propan-1-ol e ácido etanóico.
II- As moléculas do propan-1-ol, por apresentarem o grupo carboxila em sua estrutura, possuem interações moleculares mais fortes do que as moléculas do ácido etanóico.
III- O composto orgânico propan-1-ol é um álcool insolúvel em água, pois suas moléculas fazem ligações predominantemente do tipo dipolo induzido-dipolo induzido.
IV- O composto butano tem o menor ponto de ebulição, pois suas moléculas se unem por forças do tipo dipolo induzido-dipolo induzido, que são pouco intensas.
V- O composto metoxietano é um éster que apresenta em sua estrutura um átomo de oxigênio.
Das afirmações feitas está(ão) corretas:
Em uma eletrólise ígnea do cloreto de sódio, uma corrente elétrica, de intensidade igual a 5 ampères, atravessa uma cuba eletrolítica, com o auxilio de dois eletrodos inertes, durante 1930 segundos.
O volume do gás cloro, em litros, medido nas CNTP, e a massa de sódio, em gramas, obtidos nessa eletrólise, são, respectivamente:
Abaixo está representada a sua fórmula estrutural.
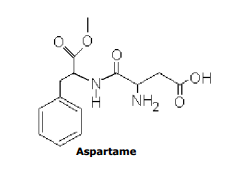
Sobre essa estrutura, são feitas as seguintes afirmações:
I- As funções orgânicas existentes na molécula dessa substância são características, apenas, de éter, amina, amida, ácido carboxílico e aldeído.
II- A fórmula molecular do aspartame é C13H15N2O5.
III- A função amina presente na molécula do aspartame é classificada como primária, porque só tem um hidrogênio substituido.
IV- A molécula de aspartame possui 7 carbonos com hibridização sp3 e 4 carbonos com hibridização sp2.
V- O aspartame possui 6 ligações π(pi) na sua estrutura.
Das afirmações feitas está(ão) corretas: