Questões Militares Sobre sistemas heterogêneos: produto de solubilidade (kps). em química
Foram encontradas 20 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Uma solução aquosa saturada em fosfato de estrôncio [Sr3(PO4)2] está em equilíbrio químico à temperatura de 25 °C, e a concentração de equilíbrio do íon estrôncio, nesse sistema, é de 7,5 x 10–7 mol L–1.
Considerando-se que ambos os reagentes (água e sal inorgânico) são quimicamente puros, assinale a alternativa CORRETA com o valor do pKPS(25ºC) do Sr3(PO4)2.
Dado: KPS = constante do produto de solubilidade.
Dado: Massa molecular relativa de CuCl = 99
Dado Kps(MX) = 5 x 10─12.
Ag+ (aq) + e-
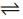 Ag(c); Eo = 0,799 e AgCl (c) + e-
Ag(c); Eo = 0,799 e AgCl (c) + e- 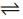 Ag(c) Cl- (aq); E = 0,222 V
Ag(c) Cl- (aq); E = 0,222 Vem que ο Eo é o potencial do eletrodo em relação ao eletrodo padrão de hidrogênio nas condições-padrão.
Considere o produto de solubilidade (K ps), a 25 0C , das substâncias I II e III:
I. Cα (OH)2; K ps = 5,0 × 10 −6II. Mg (OH)2; K ps = 5,6 × 10 −12
III . Zn (OH)2; K ps = 3,0 × 10 −17