Questões Militares Sobre teoria atômica: modelo atômico de dalton, thomson, rutherford, rutherford-bohr em química
Foram encontradas 43 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Q545369
Química
Um átomo A com n elétrons, após (n −1 ) sucessivas ionizações, foi novamente ionizado de acordo com a equação A (n −1 )+ → A n + + 1 e − . Sabendo o valor experimental da energia de ionização deste processo, pode-se conhecer o átomo A utilizando o modelo proposto por
Q545196
Química
Para uma molécula diatômica, a energia potencial em função da distância internuclear é representada pela figura ao lado. As linhas horizontais representam os níveis de energia vibracional quanticamente permitidos para uma molécula diatômica. Uma amostra contendo um mol de moléculas diatômicas idênticas, na forma de um sólido cristalino, pode ser modelada como um conjunto de osciladores para os quais a energia potencial também pode ser representada qualitativamente pela figura. Em relação a este sólido cristalino, são feitas as seguintes proposições:
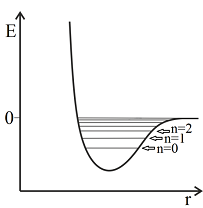
I. À temperatura de 0 K, a maioria dos osciladores estará estado vibracional fundamental, cujo número quântico vibracional, n, é igual a zero.
II. À temperatura de 0 K, todos os osciladores estarão no estado vibracional fundamental, cujo número quântico vibracional, n, é igual a zero.
III. O movimento vibracional cessa a 0 K.
IV. O movimento vibracional não cessa a 0 K.
V. O princípio de incerteza de Heisenberg será violado se o movimento vibracional cessar.
Das proposições acima estão CORRETAS
Q536992
Química
O "princípio de exclusão de Pauli" determina que cada
orbital atômico não pode ser ocupado por mais de dois
elétrons e que dois elétrons em um átomo não podem ter o
mesmo conjunto de números quânticos. Sendo assim, qual ê o
elemento químico correspondente ao átomo que possui um único
elétron no orbital mais energético com o seguinte conjunto
de números quânticos: {n=4, 1 = 2, ml = -1 e ms = +1/2}?
Ano: 2014
Banca:
CESPE / CEBRASPE
Órgão:
CBM-CE
Prova:
CESPE - 2014 - CBM-CE - Aspirante do Corpo de Bombeiros |
Q360643
Química
Metais pirofóricos, como sódio (Na), zinco (Zn), magnésio (Mg), potássio (K), bário (Ba), cálcio (Ca), alumínio (Al), zircônio (Zr) e titânio (Ti), podem sofrer ignição instantânea ao entrarem em contato com umidade ou oxigênio e causar incêndios classificados como de classe D. Portanto esses metais devem ser estocados em atmosfera inerte ou em óleos minerais. O potássio, por exemplo, reage explosivamente com água, devido à liberação de hidrogênio. O bário, ao ser queimado, forma chamas coloridas de altíssimas temperaturas. As equações químicas não balanceadas, apresentadas a seguir, ilustram esses processos. K( s) + H2O( l) → KOH( aq) + H2(g) Ba(s) + O2(g) → BaO(s)
Para combater a classe de incêndios gerados por esses materiais, deve-se empregar um extintor de pó químico elaborado à base de cloreto de sódio (NaCl).
Considerando o texto acima e os múltiplos aspectos que ele suscita, julgue os itens a seguir, utilizando, caso necessário, a tabela periódica inserida no final deste caderno de provas.
A concepção de átomo proposta por Rutherford permite explicar a coloração da chama emitida no processo de combustão do bário.
Para combater a classe de incêndios gerados por esses materiais, deve-se empregar um extintor de pó químico elaborado à base de cloreto de sódio (NaCl).
Considerando o texto acima e os múltiplos aspectos que ele suscita, julgue os itens a seguir, utilizando, caso necessário, a tabela periódica inserida no final deste caderno de provas.
A concepção de átomo proposta por Rutherford permite explicar a coloração da chama emitida no processo de combustão do bário.
Ano: 2011
Banca:
CESPE / CEBRASPE
Órgão:
CBM-DF
Prova:
CESPE - 2011 - CBM-DF - Aspirante do Corpo de Bombeiro |
Q266734
Química
O conceito de átomo nuclear, que diz respeito à estrutura constituída de um núcleo denso carregado positivamente e de uma região externa, pouco densa, na qual se localizam os elétrons, foi desenvolvido por Thomson, com base em experimentos com raios catódicos.

