Questões Militares
Foram encontradas 510 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Foram misturados sob agitação Ag2S sólido e uma solução de saturada de H2S (0,1 mol/L) em H+ (0,15 mol/L).
Considerem-se as constantes de equilíbrio a 25 ºC:
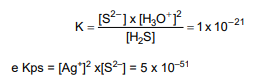
Nessa temperatura, ao se atingir o equilíbrio, a concentração de íons Ag+ na solução será:
Um procedimento para obtenção de estanho metálico foi realizado a partir do óxido de estanho (IV), em um compartimento selado que, após ser evacuado, foi preenchido com gás hidrogênio. Ao ser atingido o equilíbrio químico a 900 K, a atmosfera gasosa no interior do compartimento era composta por 45% gás hidrogênio, em volume.
A constante de equilíbrio, Kp, para essa reação a 900 K é igual a, aproximadamente,
A fosfina, PH3 , é uma substância gasosa em temperatura ambiente que pode ser obtida a partir da reação do fosfeto de cálcio sólido com água. Nessa reação, forma-se também o hidróxido de cálcio.
Uma certa massa de fosfeto de cálcio foi adicionada em água em um béquer aberto totalizando uma mistura reacional com massa igual a 1.000 g. Ao término da reação com consumo total do fosfeto de cálcio, a massa da mistura no interior do béquer era igual a 796 g.
A massa de água da mistura reacional no béquer era igual a
Três líquidos foram aquecidos em recipientes abertos, sob as mesmas condições de taxa de aquecimento e de pressão ambiente. O líquido 1 é água destilada; o líquido 2 é uma solução aquosa de cloreto de potássio 0,1 mol/L; e o líquido 3 é uma solução aquosa de nitrato de alumínio 0,1 mol/L.
Ao atingirem a temperatura de ebulição, comparando-se suas pressões de vapor, tem-se, corretamente, que:


2 H2(g) + O2(g) → 2 H2O(g)
Nessa reação, o hidrogênio reage com o oxigênio em proporção 1:8 (em massa).
A esse respeito, analise as afirmativas a seguir.
I. A combustão completa de 5g de hidrogênio requer 40g de oxigênio.
II. A mistura de 4g de hidrogênio com 16g de oxigênio deverá gerar 20g de água.
III. A combustão de 2g de hidrogênio gera 2g de água.
Está correto o que se afirma em