Questões Militares
Foram encontradas 813 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
MnO4 – (aq) + H2 O2 (aq) + H+ (aq) → Mn2+ (aq) + O2 (g) + H2 O(l)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2 O2 ; E0 = + 0,68 V MnO4 – (aq) + 8 H+ (aq) + 5 e– → Mn2+(aq) + 4 H2 O(l); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
A pirâmide olfativa usada na formulação de perfumes considera a volatilidade das substâncias.
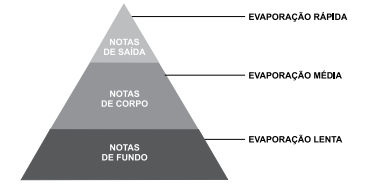
(O que significa no perfume as notas de saída, corpo e fundo? Moda Masculina Journal. Adaptado)
A tabela reúne a pressão de vapor de algumas substâncias a 25 ºC e respectivos aromas.
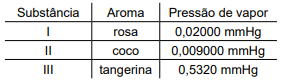
De acordo com as informações fornecidas, pode-se concluir que é nota de saída, de corpo e de fundo, respectivamente,
2 H2 S(g) + 3 O2 (g) → 2 SO2 (g) + 2 H2 O(g)
A tabela reúne as entalpias de formação dos componentes da reação.

Portanto, a entalpia da reação, em kJ.mol–1 de H2 S(g), é, aproximadamente,
Na + CH3 CH2 OH → CH3 CH2 ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,