Questões Militares
Foram encontradas 525 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
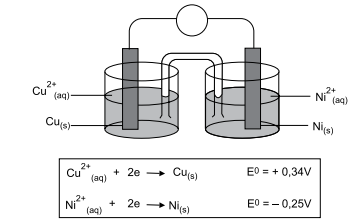
Considerando a constante de Faraday igual a 9,65 × 104 C.mol–1 , a energia livre de Gibbs para essa pilha é
MnO4 – (aq) + H2 O2 (aq) + H+ (aq) → Mn2+ (aq) + O2 (g) + H2 O(l)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2 O2 ; E0 = + 0,68 V MnO4 – (aq) + 8 H+ (aq) + 5 e– → Mn2+(aq) + 4 H2 O(l); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
2 H2 S(g) + 3 O2 (g) → 2 SO2 (g) + 2 H2 O(g)
A tabela reúne as entalpias de formação dos componentes da reação.

Portanto, a entalpia da reação, em kJ.mol–1 de H2 S(g), é, aproximadamente,
Considere a estrutura a seguir:
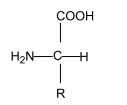
A estrutura química representada é a fórmula geral dos ______________ . A formação de cadeia polimérica dessas estruturas se dá por _________, formando um ___________.
As lacunas são preenchidas, correta e respectivamente,
por:
A reação a seguir representa uma reação de substituição nucleofílica.
2 CH3 OH + (CH3 )3 CCl → (CH3) 3 COCH3 + CH3 OH2 + + Cl-
Nessa reação, o nome do reagente oxigenado e a função
orgânica do produto não iônico são, respectivamente