Questões da Prova Marinha - 2011 - CAP - Cabo - Técnico em Química
Foram encontradas 12 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Observe o gráfico a seguir.
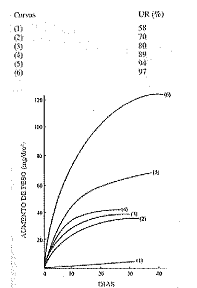
O gráfico acima evidencia a influência de deposição de partículas de NaCl em superfícies de ferro, em diferentes valores de umidade relativa.
Analisando o gráfico, é correto afirmar que
Coloque F (falso) ou V (verdadeiro)nas afirmativas abaixo, em relação à potenciometria, assinalando, a seguir, a opção correta.
I - Potenciometria é uma aplicação analítica direta da equação de Nernst, medindo-se os potenciais de elétrodos polarizados em condições de corrente zero.
II - A equação de Nernst fornece uma relação simples entre o potencial relativo de um elétrodo e a concentração das espécies iônicas correspondentes em solução.
III- O mais importante elétrodo sensível ao pH é o elétrodo de vidro. Esse dispositivo se baseia no fato de membranas delgadas de certas variedades de vidro serem suscetíveis aos íons-hidrogênio.
Um sistema com volume de 25 litros absorve 1 KJ de calor. Qual a variação de energia quando o sistema se expande para um volume de 29 litros, contra uma pressão constante externa de 1 atm?
Considere:
calor absorvido pelo sistema (+ ) ;
Calor perdido pelo sistema (-) ;
Trabalho realizado pelo sistema (-) ;
Trabalho realizado sobre o sistema (+ ) ; e
1 l.atm = 100 J
Calcule a entalpia padrão de combustão de glicose, e assinale a opção correta.
Dados:
C6H12O6 (s) ΔH formação = -1268 KJ/mol
CO2 (g) ΔH formação = -393 KJ/mol
H2O (1) ΔH formação = -286 KJ/mol