Questões de Concurso Militar EsFCEx 2023 para Oficial - Magistério em Química
Foram encontradas 4 questões
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260534
Química
Texto associado
A maior parte da produção industrial do magnésio é obtida a partir da água do mar, onde o elemento químico
magnésio se encontra na forma de íons Mg2+
(aq), em
concentração média de 1,3 g.L–1
. O processo segue as
seguintes etapas:
I. Precipitação de Mg(OH)2 por adição de cal viva.
II. Conversão a MgCl2 por adição de HCl.
III. Eletrólise ígnea do MgCl2.
Sabendo que a constante de Faraday é 9,65×104
C.mol–1
,
a quantidade de carga elétrica necessária para obter todo
o magnésio contido em 1 m3
de água do mar é de, aproximadamente,
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260544
Química
A mistura entre íons permanganato e peróxido, em meio ácido, pode ser representada pela seguinte equação não balanceada:
MnO4 – (aq) + H2 O2 (aq) + H+ (aq) → Mn2+ (aq) + O2 (g) + H2 O(l)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2 O2 ; E0 = + 0,68 V MnO4 – (aq) + 8 H+ (aq) + 5 e– → Mn2+(aq) + 4 H2 O(l); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
MnO4 – (aq) + H2 O2 (aq) + H+ (aq) → Mn2+ (aq) + O2 (g) + H2 O(l)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2 O2 ; E0 = + 0,68 V MnO4 – (aq) + 8 H+ (aq) + 5 e– → Mn2+(aq) + 4 H2 O(l); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260550
Química
O esquema a seguir representa o funcionamento de uma
bateria do tipo íon lítio, cuja equação global é representada pela equação:
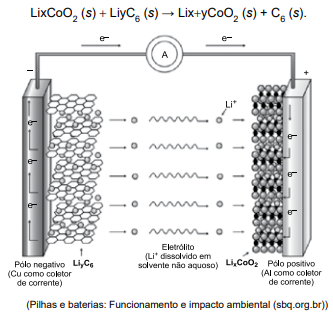
De acordo com o esquema, durante a descarga da bateria

De acordo com o esquema, durante a descarga da bateria
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260551
Química
O esquema mostra a pilha formada por eletrodos de níquel e cobre. O quadro da sequência traz os potenciais-padrão de redução desses eletrodos.
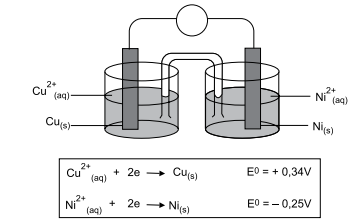
Considerando a constante de Faraday igual a 9,65 × 104 C.mol–1 , a energia livre de Gibbs para essa pilha é

Considerando a constante de Faraday igual a 9,65 × 104 C.mol–1 , a energia livre de Gibbs para essa pilha é