Questões de Concurso Militar CBM-DF 2017 para Soldado - Condutor e Operador de Viaturas - Prova Anulada
Foram encontradas 3 questões
A lei que é usada para identificar o sentido da mudança espontânea, a segunda lei da termodinâmica, também se exprime em termos de uma função de estado, a entropia. A primeira lei usa a energia interna para identificar as mudanças permitidas; a segunda lei usa a entropia para identificar as mudanças espontâneas entre as mudanças permitidas.
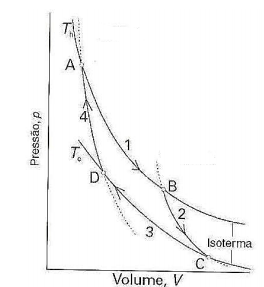
Sobre o ciclo de Carnot, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A variação de entropia é qh/Th, em que qh é a energia na forma de calor fornecida ao sistema pela fonte quente.
( ) Há troca de calor; a variação de entropia é nula.
( ) A variação de entropia do sistema é qc/Tc , qc é positivo.
( ) Não há troca térmica e, portanto, a variação de entropia é nula.
A sequência está correta em