Questões de Concurso Militar EsFCEx 2020 para Magistério de Química
Foram encontradas 4 questões
Q1778940
Química
Em um experimento foram empregados três barômetros
que continham no interior de cada um dos tubos, acima
do mercúrio, uma coluna de idêntico volume de líquido.
Em um dos tubos, o líquido era água destilada. Dois dos
líquidos eram soluções de idênticas concentrações, sendo
uma delas de cloreto de sódio e a outra de glicose. A montagem do experimento é representada na figura.
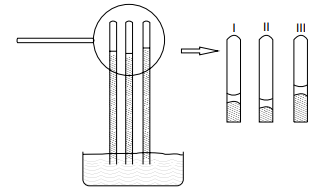
Nesse experimento, a água, a solução de cloreto de sódio e a solução de glicose estão contidas, respectivamente, nos tubos

Nesse experimento, a água, a solução de cloreto de sódio e a solução de glicose estão contidas, respectivamente, nos tubos
Q1778942
Química
Em um balão volumétrico de 100 mL foram adicionados,
com emprego de pipetas volumétricas, 5,0 mL de solução
de nitrato de alumínio 2,0 mol/L e 1,0 mL de solução de
ácido nítrico 1,0 mol/L. Completou-se o volume do balão
com água destilada.
Considerando que se empregou a técnica quantitativa na preparação da solução, a concentração de íons nitrato na solução preparada é
Considerando que se empregou a técnica quantitativa na preparação da solução, a concentração de íons nitrato na solução preparada é
Q1778943
Química
Foram misturados em um recipiente 875 g de sacarose e
350 mL de água a 70 ºC, obtendo-se uma mistura homogênea e viscosa. Essa solução foi resfriada naturalmente,
em condições ambiente, e foi mantida em repouso a 20 ºC.
Após algumas horas, foram separados os cristais de sacarose formados ao longo do período de resfriamento.
Considere a curva de solubilidade da sacarose.
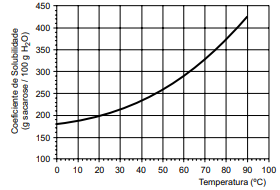
A temperatura em que se iniciou a cristalização e a massa máxima de açúcar cristalizada na solução em repouso a 20 ºC são, correta e respectivamente,
Considere a curva de solubilidade da sacarose.

A temperatura em que se iniciou a cristalização e a massa máxima de açúcar cristalizada na solução em repouso a 20 ºC são, correta e respectivamente,
Q1778946
Química
Considere as reações ácido-base representadas nas
equações:
I. NH4+ + NH2– → 2NH3. II. CH3NH2 + H2O → CH3NH3+ + OH– III. SO3 2– + S → S2O3 2–
As espécies que atuam como ácido nas reações representadas em I, II e III são, respectivamente,
I. NH4+ + NH2– → 2NH3. II. CH3NH2 + H2O → CH3NH3+ + OH– III. SO3 2– + S → S2O3 2–
As espécies que atuam como ácido nas reações representadas em I, II e III são, respectivamente,