Questões do Enem
Foram encontradas 102 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O elemento iodo (I) tem função biológica e é acumulado na tireoide. Nos acidentes nucleares de Chernobyl e Fukushima, ocorreu a liberação para a atmosfera do radioisótopo 131I, responsável por enfermidades nas pessoas que foram expostas a ele. O decaimento de uma massa de 12 microgramas do isótopo 131I foi monitorado por 14 dias, conforme o quadro.
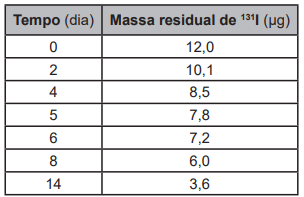
Após o período de 40 dias, a massa residual desse
isótopo é mais próxima de
Um grupo de alunos realizou um experimento para observar algumas propriedades dos ácidos, adicionando um pedaço de mármore (CaCO3) a uma solução aquosa de ácido clorídrico (HCl), observando a liberação de um gás e o aumento da temperatura.
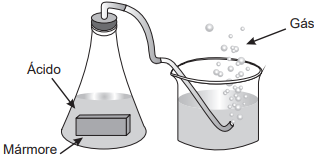
O gás obtido no experimento é o:

Um marceneiro esqueceu um pacote de pregos ao relento, expostos à umidade do ar e à chuva. Com isso, os pregos de ferro, que tinham a massa de 5,6 g cada, acabaram cobertos por uma camada espessa de ferrugem (Fe2O3 ˑ H2O), uma substância marrom insolúvel, produto da oxidação do ferro metálico, que ocorre segundo a equação química:
2 Fe (s) + 3/2 O2 (g) + H2O (l) → Fe2O3 ˑ H2O (s)
Qual foi a massa de ferrugem produzida ao se oxidar a
metade (50%) de um prego?
A presença de substâncias ricas em enxofre em áreas de mineração provoca preocupantes impactos ambientais. Um exemplo dessas substâncias é a pirita (FeS2), que, em contato com o oxigênio atmosférico, reage formando uma solução aquosa ferruginosa, conhecida como drenagem ácida de minas, segundo a equação química:
4 FeS2 (s) + 15 O2 (g) + 2 H2O (l) → 2 Fe2 (SO4 )3 (aq) + 2 H2SO4 (aq)
Em situações críticas, nas quais a concentração do ácido sulfúrico atinge 9,8 g/L, o pH alcança valores menores que 1,0. Uma forma de reduzir o impacto da drenagem ácida de minas é tratá-la com calcário (CaCO3). Considere que uma amostra comercial de calcário, com pureza igual a 50% em massa, foi disponibilizada para o tratamento.
FIGUEIREDO, B. R. Minérios e ambientes. Campinas: Unicamp, 2000 (adaptado).
Qual é a massa de calcário, em gramas, necessária para neutralizar um litro de drenagem ácida de minas, em
seu estado crítico, sabendo-se que as massas molares do CaCO3 e do H2SO4 são iguais a 100 g/mol e 98 g/mol,
respectivamente?