Questões de Vestibular Para ufrr
Foram encontradas 144 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Q1266893
Química
A Häagen-Dazs, marca Nova Yorkina, conhecida por
fabricar os melhores sorvetes do mundo, pretende lançar
uma nova linha de sabores. Para isso, a equipe técnica do
laboratório de desenvolvimento e inovação da rede estudou a estrutura de dois compostos orgânicos: o ácido
fumárico e o ácido maleico, que apresentam a mesma
fórmula molecular (C4H4O4). Como as substâncias
apresentavam estruturas diferentes, devido à isomeria
espacial, existe uma diferença na durabilidade dos sabores
finais. A estrutura correspondente ao isômero cis era
pouco favorável à durabilidade dos sorvetes e possuía
baixa atividade antioxidante, enquanto que a estrutura
correspondente ao isômero trans aumentava a
durabilidade dos sorvetes e possuía alta atividade
antioxidante. As fórmulas estruturais dessas substâncias
estão representadas a seguir: 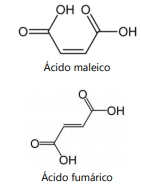
Sabendo que, na composição da nova linha de sorvetes, será utilizado o composto capaz de aumentar a validade do produto, a substância e sua justificativa de escolha são, respectivamente ácido:

Sabendo que, na composição da nova linha de sorvetes, será utilizado o composto capaz de aumentar a validade do produto, a substância e sua justificativa de escolha são, respectivamente ácido:
Q1266892
Química
A borracha de butadieno estireno, SBR, é sem dúvida
a borracha sintética mais difundida no mundo. Foi
elaborada primeiro na Alemanha, na década de 1930, com
o nome de Buna-S. Durante a 2ª Guerra Mundial, foi
estudada pelos Estados Unidos com a denominação de
GRS (Government Rubber-Styrene), sendo posteriormente
substituída por SBR. O SBR ou Buna-S é usado
principalmente nas bandas de rodagem de pneus, solados
e cabos de isolamento e sintetizado a partir dos
monômeros but-1,3-dieno e estireno (fenil-eteno).
Considere as seguintes afirmativas:
I. O but-1,3-dieno apresenta cadeia aberta e insaturada. II. Ambos os monômeros são hidrocarbonetos. III. O but-1,3-dieno pode apresentar isômeros planos de posição, como o but-1,4-dieno. IV. O fenil-eteno apresenta isômeros de posição.
Nesse contexto, é possível afirmar que estão CORRETAS as afirmativas:
Considere as seguintes afirmativas:
I. O but-1,3-dieno apresenta cadeia aberta e insaturada. II. Ambos os monômeros são hidrocarbonetos. III. O but-1,3-dieno pode apresentar isômeros planos de posição, como o but-1,4-dieno. IV. O fenil-eteno apresenta isômeros de posição.
Nesse contexto, é possível afirmar que estão CORRETAS as afirmativas:
Q1266891
Química
O ácido acetilsalicílico (AAS), componente principal da
aspirina, é um medicamento tomado por milhões de
pessoas, e geralmente sem prescrição médica, para aliviar
as dores. Por ser um ácido, a aspirina sofre ionização em
meio aquoso, estabelecendo o seguinte equilíbrio
químico:
AAS (s) + H2O (l) ⇄ AAS‾ (aq) + H3O+ (aq)
Assim, quando se toma um medicamento que contém o AAS com um pouco de água, a maior parte do medicamento encontra-se na forma ionizada (AAS‾ ) e nesta forma ela não atravessa a camada protetora das paredes do estômago. A forma neutra (AAS) pode atravessar as paredes do estômago causando hemorragia em algumas pessoas ou outras complicações médicas.
Sobre o equilíbrio químico do AAS em nosso organismo, é CORRETO afirmar que:
AAS (s) + H2O (l) ⇄ AAS‾ (aq) + H3O+ (aq)
Assim, quando se toma um medicamento que contém o AAS com um pouco de água, a maior parte do medicamento encontra-se na forma ionizada (AAS‾ ) e nesta forma ela não atravessa a camada protetora das paredes do estômago. A forma neutra (AAS) pode atravessar as paredes do estômago causando hemorragia em algumas pessoas ou outras complicações médicas.
Sobre o equilíbrio químico do AAS em nosso organismo, é CORRETO afirmar que:
Q1266890
Química
Para estudar os efeitos da cafeína na execução de
exercícios físicos, um grupo de estudantes de Ciências do
Esporte da Universidade de Northumbria, no Reino Unido,
decidiu fazer um experimento: dois voluntários deveriam
ingerir, cada um, 0,3 g de cafeína. No entanto, o estudo quase se transformou em tragédia quando um erro de
cálculo na dosagem da substância levou os dois
estudantes ao hospital. Para calcular a dosagem para cada estudante,
funcionários da universidade utilizaram a calculadora de
um telefone celular, mas erraram ao digitar as casas
decimais. Cada estudante ingeriu 30 g de cafeína
dissolvidos em suco de laranja - o equivalente a 300
xícaras de café. Os dois jovens sofreram violentos efeitos colaterais.
Ambos precisaram fazer tratamento de diálise, mas se
recuperaram. Segundo a universidade, o experimento foi
realizado sem a supervisão adequada.
Texto adaptado de http://g1.globo.com/ciencia-e-saude/noticia/erro-decalculo-em-experimento-deixa-2-estudantes-de-ciencia-na-uti-porexcesso-de-cafeina.ghtml Acesso em 15 de abril de 2017.
Sabendo que a massa de cafeína (C8H10O2N4) foi dissolvida em 100 mL de suco de laranja, a concentração de cafeína ingerida por cada estudante foi aproximadamente de
Texto adaptado de http://g1.globo.com/ciencia-e-saude/noticia/erro-decalculo-em-experimento-deixa-2-estudantes-de-ciencia-na-uti-porexcesso-de-cafeina.ghtml Acesso em 15 de abril de 2017.
Sabendo que a massa de cafeína (C8H10O2N4) foi dissolvida em 100 mL de suco de laranja, a concentração de cafeína ingerida por cada estudante foi aproximadamente de
Q1266889
Química
Considere uma pilha de combustível no qual o
funcionamento é baseado nas semi-reações abaixo, cada
uma delas representada com o respectivo potencial
padrão de redução:
2 H2O + 2 e- → H2 + 2 OH- E° = - 0,828 V ½ O2 + H2O + 2 e- → OH- E° = + 0,401 V
Levando-se em conta essas informações e as assertivas a seguir,
I. A reação global da pilha de combustível é H2 + ½ O2 → H2O II. O hidrogênio sofre oxidação no processo. III. A diferença de potencial da pilha de combustível, em condição padrão, é igual a 1,229 V. IV. O gás oxigênio (O2) é o agente redutor.
Pode-se afirmar que estão CORRETAS apenas:
2 H2O + 2 e- → H2 + 2 OH- E° = - 0,828 V ½ O2 + H2O + 2 e- → OH- E° = + 0,401 V
Levando-se em conta essas informações e as assertivas a seguir,
I. A reação global da pilha de combustível é H2 + ½ O2 → H2O II. O hidrogênio sofre oxidação no processo. III. A diferença de potencial da pilha de combustível, em condição padrão, é igual a 1,229 V. IV. O gás oxigênio (O2) é o agente redutor.
Pode-se afirmar que estão CORRETAS apenas: