Questões da Prova PUC - SP - 2016 - PUC - SP - Vestibular- Primeiro Semestre
Foram encontradas 81 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
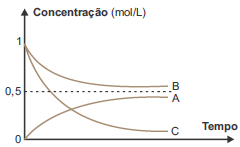
A respeito do experimento, foram feitas algumas afirmações:
I. A e B são reagentes e C é o produto da reação estudada. II. A reação química estudada é corretamente representada pela equação: B + 2 C → A III. Não houve consumo completo dos reagentes, sendo atingido o equilíbrio químico. IV. A constante de equilíbrio dessa reação, no sentido da formação de A, nas condições do experimento é menor do que 1.
Estão corretas apenas as afirmações:
A análise de um composto orgânico oxigenado de fórmula geral Cx Hy Oz permitiu uma série de informações sobre o comportamento químico da substância.
I. A combustão completa de uma amostra contendo 0,01 mol desse composto forneceu 1,76 g de CO2 e 0,72 g de água.
II. Esse composto não sofre oxidação em solução de KMnO4 em meio ácido.
III. A redução desse composto fornece um álcool.
Com base nessas afirmações é possível deduzir que o
nome do composto é
A tabela a seguir sintetiza os dados experimentais obtidos de um estudo cinético da reação.

A expressão da equação da velocidade nas condições dos experimentos é
Dados:

São conhecidos alguns radioisótopos dos elementos polônio e rádio.
Em um experimento, duas amostras de massas diferentes, uma de polônio-208 e outra de rádio-224, foram mantidas em uma caixa de chumbo por 18 anos. Ao final desse período, verificou-se que a massa de cada um desses radioisótopos presente no recipiente era igual a 0,025 mg.
Sobre esse experimento foram feitas algumas observações:
I. A desintegração β do 224Ra resulta no isótopo 224Pa.
II. A desintegração α do 208Po resulta no isótopo 204Pb.
III. A massa inicial de 224Ra na caixa de chumbo era de 0,200 mg. 208
IV. A massa inicial de 208Po na caixa de chumbo era de 0,150 mg.
Estão corretas apenas as afirmações:
Dado:

A reação de hidrogenação do etileno ocorre com aquecimento, na presença de níquel em pó como catalisador. A equação termoquímica que representa o processo é
C2 H4 (g) + H2 (g) → C2 H6 (g) ΔHθ = - 137 kJ.mol-1
