Questões da Prova FGV - 2014 - FGV - Vestibular - 1° Fase - Prova Tarde- 2015
Foram encontradas 60 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A utilidade do combustível X pode ser vinculada às suas propriedades, como o alto poder calorífico por unidade de massa, já que o calor resultante da sua queima aquece caldeiras, que geram vapor, que movimentam turbinas, que geram energia elétrica. O gás produzido por esse combustível pode resultar em fertilizantes, amônia, combustíveis líquidos, lubrificantes, combustível para aviação e isqueiros, metanol, etc
(https://sistemas.dnpm.gov.br/publicacao/mostra_ imagem.asp?IDBancoArquivoArquivo=3970. Adaptado)
O combustível X descrito no texto é
O surto da doença ebola já atinge vários países da África, causando centenas de mortes. O Japão pode oferecer uma medicação, o favipiravir. Entretanto, ela ainda não recebeu aprovação para uso.
(http://info.abril.com.br/noticias/ciencia/2014/08/japao-pode-oferecermedicamento-sem-aprovacao-para-ebola.shtml. Adaptado)
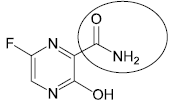
Na molécula do favipiravir, o número total de átomos de carbono
que fazem ligações do tipo π e o grupo funcional destacado
na estrutura são, respectivamente:
P4 + H2O → PH3 + H3PO4
A soma dos menores valores inteiros dos coeficientes estequiométricos dessa equação corretamente balanceada é igual a
Fontes alternativas de energia têm sido foco de interesse global como a solução viável para crescentes problemas do uso de combustíveis fósseis. Um exemplo é a célula a combustível microbiológica que emprega como combustível a urina. Em seu interior, compostos contidos na urina, como ureia e resíduos de proteínas, são transformados por micro-organismos que constituem um biofilme no anodo de uma célula eletroquímica que produz corrente elétrica.
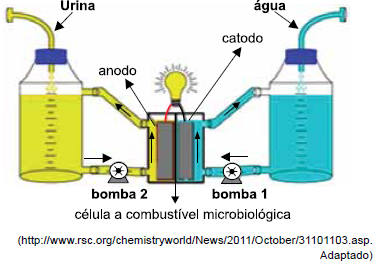
Sobre essa célula eletroquímica, é correto afirmar que, quando
ela entra em operação com a geração de energia elétrica, o
biofilme promove a
Estudos ambientais revelaram que o ferro é um dos metais presentes em maior quantidade na atmosfera, apresentando- -se na forma do íon de ferro 3+ hidratado, [Fe(H2 O)6 ] 3+. O íon de ferro na atmosfera se hidrolisa de acordo com a equação
[Fe(H2 O)6 ] 3+ ↔ [Fe(H2 O)5 OH]2+ + H+
(Química Nova, vol. 25, n.º 2, 2002. Adaptado) Um experimento em laboratório envolvendo a hidrólise de íons de ferro em condições atmosféricas foi realizado em um reator de capacidade de 1,0 L. Foi adicionado inicialmente 1,0 mol de [Fe(H2 O6 ) ]3+ e, após a reação atingir o equilíbrio, havia sido formado 0,05 mol de íons H+. A constante de equilíbrio dessa reação nas condições do experimento tem valor aproximado igual a