Questões de Vestibular
Foram encontradas 967 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2023
Banca:
COMVEST - UNICAMP
Órgão:
UNICAMP
Prova:
COMVEST - UNICAMP - 2023 - UNICAMP - Vestibular - Conhecimentos Gerais - 1ª Fase |
Q2327089
Química
Algumas baterias transformam certas substâncias em outras,
gerando energia elétrica. Isso permite, por exemplo, o funcionamento de equipamentos tendo como base essa energia (carros
elétricos) ou então auxilia o funcionamento de equipamentos
(carros de combustão interna). É por isso que os carros elétricos
precisam se abastecer de energia elétrica de tempos em tempos
e os de combustão não, já que a bateria desses últimos é carregada durante seu funcionamento. Na descarga da bateria, dois
comportamentos são importantes: curva de tensão (Figura A) e
ciclo de vida (Figura B), sendo esse último a quantidade de vezes
que a bateria pode ser recarregada em função da profundidade
de sua descarga.
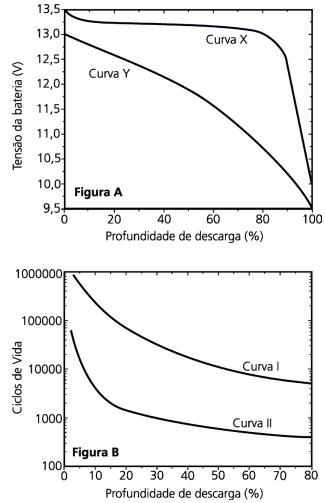
Levando em conta essas informações, seria apropriado escolher para equipar um carro

Levando em conta essas informações, seria apropriado escolher para equipar um carro
Ano: 2023
Banca:
UERJ
Órgão:
UERJ
Prova:
UERJ - 2023 - UERJ - Vestibular Estadual 2024 – 1º Exame de Qualificação |
Q2182204
Química
Para aumentar a eficiência energética de uma caldeira industrial, pesquisadores realizaram um
teste que verificou a expansão volumétrica de uma amostra de gás ideal em função da temperatura.
Observe os resultados no gráfico:
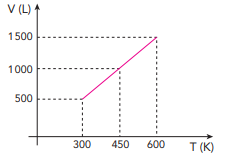
Admita que o processo de expansão volumétrica ocorre à pressão constante de 8 atm e que a constante universal dos gases ideais é de 0,08 atm.L/mol.K. Ao atingir a temperatura máxima, o número de mols da amostra de gás corresponderá a:

Admita que o processo de expansão volumétrica ocorre à pressão constante de 8 atm e que a constante universal dos gases ideais é de 0,08 atm.L/mol.K. Ao atingir a temperatura máxima, o número de mols da amostra de gás corresponderá a:
Ano: 2023
Banca:
UERJ
Órgão:
UERJ
Prova:
UERJ - 2023 - UERJ - Vestibular Estadual 2024 – 1º Exame de Qualificação |
Q2182201
Química
Observe a equação química que representa a hidrólise do carbeto de cálcio.
CaC2 (s) + 2 H2 O (l) → Ca(OH)2 (aq) + C2 H2 (g)
O nome do composto orgânico obtido nessa reação é:
CaC2 (s) + 2 H2 O (l) → Ca(OH)2 (aq) + C2 H2 (g)
O nome do composto orgânico obtido nessa reação é:
Ano: 2023
Banca:
PUC - RS
Órgão:
PUC - RS
Provas:
PUC - RS - 2022 - PUC - RS - Vestibular - Primeiro Semestre - Medicina
|
PUC - RS - 2023 - PUC - RS - Vestibular - Medicina |
Q2092745
Química
O Acordo de Paris tem por objetivo alcançar a descarbonização do planeta e estabelece como meta limitar o aumento
da temperatura global a 1,5 ºC. Nesse contexto, o hidrogênio verde mostra-se como uma alternativa promissora por
tratar-se de um vetor energético obtido a partir de tecnologia limpa.
O processo de obtenção do hidrogênio verde consiste na decomposição de moléculas de água em oxigênio e hidrogênio por meio da eletrólise, usando energias renováveis, conforme mostra a figura a seguir.
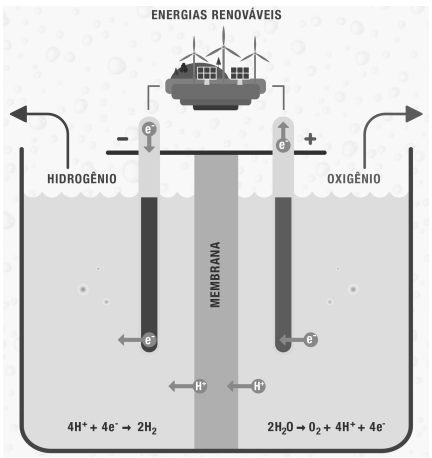
Adaptado de https://www.iberdrola.com/sustentabilidade/hidrogenio-verde.
Com base no processo eletrolítico apresentado na figura, assinale a alternativa correta.
O processo de obtenção do hidrogênio verde consiste na decomposição de moléculas de água em oxigênio e hidrogênio por meio da eletrólise, usando energias renováveis, conforme mostra a figura a seguir.

Adaptado de https://www.iberdrola.com/sustentabilidade/hidrogenio-verde.
Com base no processo eletrolítico apresentado na figura, assinale a alternativa correta.
Ano: 2023
Banca:
PUC - RS
Órgão:
PUC - RS
Provas:
PUC - RS - 2022 - PUC - RS - Vestibular - Primeiro Semestre - Medicina
|
PUC - RS - 2023 - PUC - RS - Vestibular - Medicina |
Q2092741
Química
O clorofórmio (CHCl3) foi introduzido como anestésico em procedimentos cirúrgicos no século XIX, na
Inglaterra. Entretanto, o seu uso foi gradativamente
abandonado devido ao seu alto grau de toxicidade,
sendo substituído por substâncias anestésicas mais
adequadas. O clorofórmio pode ser preparado pela
reação de metano com cloro:
CH4(g) + 3 Cl2(g) → CHCl3(l) + 3 HCl(g)
A quantidade de cloro, em gramas, necessária para produzir 1,5 mol de clorofórmio é
CH4(g) + 3 Cl2(g) → CHCl3(l) + 3 HCl(g)
A quantidade de cloro, em gramas, necessária para produzir 1,5 mol de clorofórmio é