Questões de Vestibular
Foram encontradas 438 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2015
Banca:
UNICENTRO
Órgão:
UNICENTRO
Prova:
UNICENTRO - 2015 - UNICENTRO - VESTIBULAR DE 2016 - Química |
Q1799728
Química
As reações nucleares envolvem transformações de núcleos atômicos, produzindo uma grande quantidade
de energia. Na desintegração do elemento 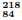 Po, as etapas sucessivas a seguir são observadas.
Po, as etapas sucessivas a seguir são observadas.
I.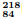 Po → α + W II. W → β + R
Po → α + W II. W → β + R
Com base nessas informações e nos conhecimentos sobre radioatividade, assinale a alternativa que indica, corretamente, o número de nêutrons que o núcleo do elemento R apresenta.
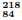 Po, as etapas sucessivas a seguir são observadas.
Po, as etapas sucessivas a seguir são observadas.
I.
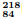 Po → α + W II. W → β + R
Po → α + W II. W → β + R
Com base nessas informações e nos conhecimentos sobre radioatividade, assinale a alternativa que indica, corretamente, o número de nêutrons que o núcleo do elemento R apresenta.
Ano: 2015
Banca:
UNICENTRO
Órgão:
UNICENTRO
Prova:
UNICENTRO - 2015 - UNICENTRO - VESTIBULAR DE 2016 - Química |
Q1799725
Química
Considere os dados a seguir a 25 ºC e 1 atm.
Substância Entalpia de formação (kcal/mol) CO2 −95,0 CO −25,0
Com base nessas informações e nos conhecimentos sobre termoquímica, assinale a alternativa que apresenta, corretamente, a entalpia da reação C(s) + CO2(g) → 2CO(g).
Substância Entalpia de formação (kcal/mol) CO2 −95,0 CO −25,0
Com base nessas informações e nos conhecimentos sobre termoquímica, assinale a alternativa que apresenta, corretamente, a entalpia da reação C(s) + CO2(g) → 2CO(g).
Ano: 2015
Banca:
UNICENTRO
Órgão:
UNICENTRO
Prova:
UNICENTRO - 2015 - UNICENTRO - VESTIBULAR DE 2016 - Química |
Q1799724
Química
As reações de oxirredução estão presentes nas mais diversas situações do nosso cotidiano, nos processos de fotossíntese, nas pilhas e baterias usadas em equipamentos elétricos e indústria metalúrgica.
Com base no texto e nos conhecimentos sobre reações de oxirredução, considere as afirmativas a seguir.
I. O número de oxidação de qualquer elemento, ao formar uma substância simples, é zero. II. Agente redutor é a substância ou elemento que, após a reação, apresenta um número de oxidação maior. III. Agente oxidante é a substância que contém o elemento que sofre oxidação. IV. A soma algébrica dos números de oxidação de todos os átomos em um íon é zero.
Assinale a alternativa correta.
Com base no texto e nos conhecimentos sobre reações de oxirredução, considere as afirmativas a seguir.
I. O número de oxidação de qualquer elemento, ao formar uma substância simples, é zero. II. Agente redutor é a substância ou elemento que, após a reação, apresenta um número de oxidação maior. III. Agente oxidante é a substância que contém o elemento que sofre oxidação. IV. A soma algébrica dos números de oxidação de todos os átomos em um íon é zero.
Assinale a alternativa correta.
Q1797137
Química
Ao se casar, um químico decidiu utilizar a
galvanoplastia para reaproveitar sua aliança de prata,
fazendo o depósito de uma camada de ouro sob a
prata. Para isso, o químico possui apenas 17,5 g de
brometo de ouro (III). Para a produção de 200 mL de
solução de brometo de ouro (III), utilizando toda a
massa que possui, qual será a concentração da
solução obtida?
Dados: Massas molares em g.mol−1 : Au = 197; Br = 80.
Dados: Massas molares em g.mol−1 : Au = 197; Br = 80.
Q1797136
Química
Uma das funções da Lei Seca no Brasil é coibir o
consumo de bebidas alcoólicas ao dirigir. Um dos
primeiros bafômetros criados (dispositivo utilizado para
a medição do teor alcoólico ingerido pelo motorista) foi
baseado na reação do etanol com o dicromato de
potássio em meio ácido, de acordo com a reação
química que está descrita a seguir.
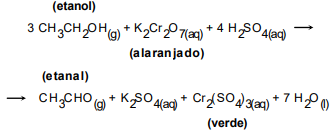
Após a reação redox, ocorre uma mudança de coloração promovida pelos compostos de cromo (Cr), levando à formação do etanal. Com base na equação química acima, qual é o número de oxidação do cromo (Cr) nos compostos K2Cr2O7 e Cr2(SO4)3, respectivamente?
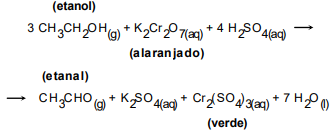
Após a reação redox, ocorre uma mudança de coloração promovida pelos compostos de cromo (Cr), levando à formação do etanal. Com base na equação química acima, qual é o número de oxidação do cromo (Cr) nos compostos K2Cr2O7 e Cr2(SO4)3, respectivamente?