Questões de Vestibular
Foram encontradas 326 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2015
Banca:
UNICENTRO
Órgão:
UNICENTRO
Prova:
UNICENTRO - 2015 - UNICENTRO - VESTIBULAR DE 2016 - Química |
Q1799725
Química
Considere os dados a seguir a 25 ºC e 1 atm.
Substância Entalpia de formação (kcal/mol) CO2 −95,0 CO −25,0
Com base nessas informações e nos conhecimentos sobre termoquímica, assinale a alternativa que apresenta, corretamente, a entalpia da reação C(s) + CO2(g) → 2CO(g).
Substância Entalpia de formação (kcal/mol) CO2 −95,0 CO −25,0
Com base nessas informações e nos conhecimentos sobre termoquímica, assinale a alternativa que apresenta, corretamente, a entalpia da reação C(s) + CO2(g) → 2CO(g).
Ano: 2016
Banca:
UNICENTRO
Órgão:
UNICENTRO
Prova:
UNICENTRO - 2016 - UNICENTRO - Vestibular - PAC - 1ª Etapa |
Q1798898
Química
Com objetivo de comprovar a Lei de Conservação das Massas
em uma reação química — Lei de Lavoisier —, um béquer de
125,0mL, contendo uma solução diluída de ácido sulfúrico, H2SO4(aq), foi pesado juntamente com um vidro de relógio,
contendo pequena quantidade de carbonato de potássio, K2CO3(s), que, em seguida, foi adicionado à solução ácida.
Terminada a reação, o béquer com a solução e o vidro de
relógio vazio foram pesados, verificando-se que a massa final,
no experimento, foi menor que a massa inicial.
Considerando-se a realização desse experimento, a conclusão correta para a diferença verificada entre as massas final e inicial é
Considerando-se a realização desse experimento, a conclusão correta para a diferença verificada entre as massas final e inicial é
Q1797133
Química
Devido à alta dureza e ao elevado valor agregado do
carbono diamante (Cdiam), a conversão do carbono
grafite (Cgraf) em carbono diamante é algo viável em
termos comerciais, a partir da aplicação de alta
temperatura e pressão. Desta forma, o cálculo da
entalpia de reação para essa transformação pode ser
realizado a partir das reações de formação do gás
carbônico a partir do Cgraf e do Cdiam, expressas abaixo:
Cgraf + O2(g) → CO2(g) = -393,3 kJ Cdiam + O2(g) → CO2(g)
= -393,3 kJ Cdiam + O2(g) → CO2(g)  = -395,2 kJ Cgraf → Cdiam
= -395,2 kJ Cgraf → Cdiam  = ?
= ?
A partir dos valores de entalpia de formação do CO2, qual é a entalpia de reação para a transformação do carbono grafite em carbono diamante?
Cgraf + O2(g) → CO2(g)
 = -393,3 kJ Cdiam + O2(g) → CO2(g)
= -393,3 kJ Cdiam + O2(g) → CO2(g)  = -395,2 kJ Cgraf → Cdiam
= -395,2 kJ Cgraf → Cdiam  = ?
= ? A partir dos valores de entalpia de formação do CO2, qual é a entalpia de reação para a transformação do carbono grafite em carbono diamante?
Q1797131
Química
Na medicina veterinária, o cloreto de amônio (NH4Cl) é
utilizado como acidulante da urina com o objetivo de
evitar infecções. Para a produção do NH4Cl, é
empregada a reação do ácido clorídrico (HCl) com
amônia (NH3), representada abaixo:
HCl(aq) + NH3(aq) → NH4Cl(s)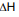 = ???
= ???
A partir dos valores das entalpias de formação do HCl ( = -46 kJ.mol-1), NH3 (
= -46 kJ.mol-1), NH3 ( = -92 kJ.mol-1) e NH4Cl (
= -92 kJ.mol-1) e NH4Cl ( = -314 kJ.mol-1), determine a variação de entalpia
(
= -314 kJ.mol-1), determine a variação de entalpia
(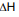 ) da reação acima e se o processo é endotérmico
ou exotérmico.
) da reação acima e se o processo é endotérmico
ou exotérmico.
HCl(aq) + NH3(aq) → NH4Cl(s)
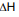 = ???
= ??? A partir dos valores das entalpias de formação do HCl (
 = -46 kJ.mol-1), NH3 (
= -46 kJ.mol-1), NH3 ( = -92 kJ.mol-1) e NH4Cl (
= -92 kJ.mol-1) e NH4Cl ( = -314 kJ.mol-1), determine a variação de entalpia
(
= -314 kJ.mol-1), determine a variação de entalpia
(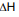 ) da reação acima e se o processo é endotérmico
ou exotérmico.
) da reação acima e se o processo é endotérmico
ou exotérmico.
Ano: 2021
Banca:
PUC-MINAS
Órgão:
PUC-MINAS
Prova:
PUC-MINAS - 2021 - PUC-MINAS - Vestibular Medicina - Caderno 1 |
Q1796708
Química
O Ciclo de Born-Haber é uma proposta para analisar a energia envolvida numa reação e foi
desenvolvido em 1917 pelos cientistas alemães Max Born e Fritz Haber.
Esse ciclo envolve a formação de um composto iônico a partir da reação de um metal com um ametal. É
utilizado, principalmente, como um método para calcular a entalpia reticular, a qual não pode ser
mensurada diretamente.
Considere o ciclo para o NaCl na figura a seguir:
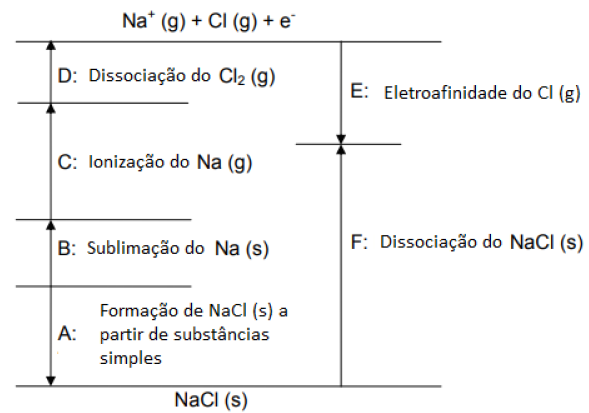
A representação CORRETA de um dos processos que ocorrem nesse ciclo é:
Considere o ciclo para o NaCl na figura a seguir:

A representação CORRETA de um dos processos que ocorrem nesse ciclo é:
