Questões de Vestibular
Foram encontradas 572 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!


Tendo como referência essas informações, julgue o item seguinte.
Quando o cálcio-41 captura um elétron, é formado o
nuclídeo 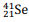 .
.
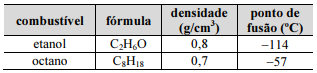
Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue os item.
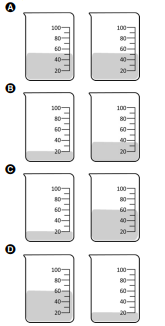
Considerando a combustão total, assinale a opção que representa corretamente os volumes dos combustíveis octano (à esquerda) e etanol (à direita) que devem ser queimados para que haja emissão de uma quantidade equivalente de CO2 pelos dois compostos.
Tendo como referência as informações precedentes, julgue o item que se segue.
O valor da variação de entalpia molar da reação em relação
à hematita, que reage com o monóxido de carbono,
produzindo apenas ferro metálico e dióxido de carbono, é
3 ΔHI + 2 ΔHII +ΔHIII.
Tendo como referência as informações precedentes, julgue o item que se segue.
Na reação III, há redução do ferro em um processo que
envolve a transferência de dois mols de elétrons por mol
de FeO.