Questões da Prova CECIERJ - 2017 - CEDERJ - Vestibular - Primeiro Semestre
Foram encontradas 8 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Em um acidente no laboratório, um frasco contendo 2.0 kg de NaOH foi quebrado e, para neutralizar essa soda foi proposta a reação
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(l),
que liberou 660 Kcal. Se 1 cal = 4.18 J, a variação da
entalpia de neutralização, em kJ mol-1, é igual a:
Com base nas informações sobre os valores de potenciais de redução, a 25º C:
Mg+2(aq) + 2 e- ⇄ Mg (s) E° = - 2.4 V
Cu+2(aq) + 2 e- ⇄ Cu (s) E° = + 0.34 V
É correto afirmar que:
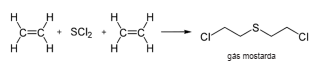
A partir da reação abaixo o volume aproximado, em metros cúbicos de etileno (d=1.18 kg/m3 ), necessário para preparar 2.0 toneladas de gás mostarda é:
O ácido láctico é um composto orgânico de função mista que apresenta fórmula CH3 CH(OH)COOH. O organismo humano produz ácido láctico em quantidades expressivas durante a realização de exercícios físicos, sendo produzido excessivamente quando esses se intensificam. No ambiente celular, o ácido láctico transforma-se em lactato, que é a sua forma ionizada. A mistura de ácido láctico e lactato de sódio, em solução aquosa, funciona como uma solução-tampão, ou seja, como, praticamente, aquela que não muda seu pH pela adição de H+ ou OH- em pequenas quantidades.
Supondo uma solução contendo 0.15 mol/L de ácido láctico e 0.15 mol/L de lactato de sódio (Ka = 1.0 x 10-4) e negligenciando a quantidade de ácido que ioniza, o valor do pH será igual a :
A Astaxantina é um carotenoide que, ao contrário de outros, não se converte em Vitamina A no corpo humano, sendo um poderoso antioxidante e componente nutricional natural.
Com massa molar de aproximadamente 596 g/mol e fórmula centesimal C (80.54%), H (8.72%) e O (10.74%), esse carotenoide é representado pela fórmula molecular: