Questões da Prova UERJ - 2010 - UERJ - Vestibular - Primeiro Exame
Foram encontradas 7 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A sigla BTEX faz referência a uma mistura de hidrocarbonetos monoaromáticos, poluentes atmosféricos de elevada toxidade.
Considere a seguinte mistura BTEX:
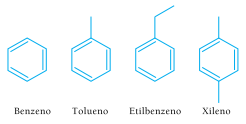
Ao fim de um experimento para separar, por destilação fracionada, essa mistura, foram obtidas três frações. A primeira e a segunda frações continham um composto distinto cada uma, e a terceira continha uma mistura dos outros dois restantes.
Os compostos presentes na terceira fração são:
As bolas de futebol são feitas, atualmente, de poliuretano, um polímero sintético cuja obtenção pode ser representada pela seguinte equação química, na qual R e R’ são cadeias de hidrocarbonetos:
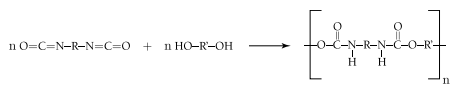
Pode-se observar, na molécula de poliuretano assim obtida, a formação de um grupo correspondente
à seguinte função química:
A massa de hidrogênio, em gramas, necessária para gerar a mesma quantidade de energia que a gerada por 1 g de dodecano equivale a:
Observe, a seguir, a fórmula estrutural do ácido ascórbico, também conhecido como vitamina C:
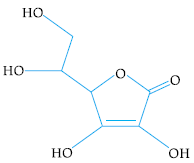
Para uma dieta saudável, recomenda-se a ingestão diária de 2,5 x 10-4 mol dessa vitamina, preferencialmente obtida de fontes naturais, como as frutas.
Considere as seguintes concentrações de vitamina C:
- polpa de morango: 704 mg.L-1;
- polpa de laranja: 528 mg.L-1.
Um suco foi preparado com 100 mL de polpa de morango, 200 mL de polpa de laranja e 700 mL de água.
A quantidade desse suco, em mililitros, que fornece a dose diária recomendada de vitamina C é:
Em um experimento, uma pequena amostra de soro sanguíneo foi colocada em um suporte poroso embebido em meio formado por solução salina mantida em pH 6,0. Através desse suporte estabeleceu-se um circuito elétrico, como mostra o esquema abaixo.

|
Proteína |
pI (valores médios) |
|
|
nome |
velocidade de migração |
|
|
gamaglobulina |
v1 |
8,0 |
|
betaglobulina |
v2 |
7,6 |
|
alfaglobulina |
v3 |
6,6 |
|
albumina |
v4 |
4,8 |
A ordem crescente das velocidades de migração das proteínas citadas é: