Questões da Prova PUC - RJ - 2016 - PUC - RJ - Vestibular - Grupo 2
Foram encontradas 20 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Na bancada de um laboratório, existem quatro soluções aquosas, cada uma contendo dissolvido um dos seguintes eletrólitos listados abaixo.
I. NaCl
II. NaOH
III. HCl
IV. CH3COONa
Considerando concentrações, em quantidade de matéria, equivalentes, as soluções teriam os valores de pH na seguinte ordem crescente:
Pedrinho tem duas caixas de brinquedos, uma grande e uma pequena. Sabemos o seguinte:
• 80% dos brinquedos estão na caixa grande,
• 10% dos brinquedos da caixa grande são vermelhos,
• 20% dos brinquedos da caixa pequena são vermelhos.
Dentre os brinquedos de Pedrinho, qual é a porcentagem de brinquedos vermelhos?
Considere as seguintes semicélulas e os respectivos potenciais-padrão de redução, numerados de I a VI.
I) Mn2+ (aq)/Mn(s) E0=-1,18 V
II) Al3+ (aq)/Al(s) E0=-1,66 V
III) Ni2+ (aq)/Ni(s) E0=-0,25 V
IV) Pb2+ (aq)/Pb(s) E0=-0,13 V
V) Ag+ (aq)/Ag(s) E0= +0,80V
VI) Cu2+ (aq)/Cu(s) E0= +0,34 V
As duas semicélulas que formariam uma pilha com maior diferença de potencial são
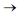 AgCl(s)
AgCl(s)