Questões de Vestibular UNIFESP 2007 para Vestibular - Conhecimentos Gerais
Foram encontradas 2 questões
Ano: 2007
Banca:
VUNESP
Órgão:
UNIFESP
Prova:
VUNESP - 2007 - UNIFESP - Vestibular - Conhecimentos Gerais |
Q218444
Química
Analgésicos ácidos como aqueles à base de ácido acetilsalicílico provocam em algumas pessoas sintomas desagradáveis associados ao aumento da acidez estomacal. Em substituição a esses medicamentos, podem ser ministrados outros que contenham como princípio ativo o paracetamol (acetaminofen), que é uma base fraca. O meio estomacal é predominantemente ácido, enquanto que o meio intestinal é predominantemente básico, o que leva à absorção seletiva nos dois órgãos de medicamentos administrados pela via oral.
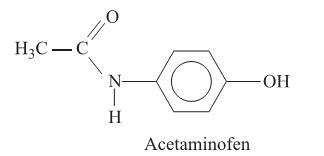
Considere a figura com a estrutura do acetaminofen e as seguintes afirmações:
I. O acetaminofen apresenta fórmula molecular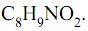
II. O grupo funcional amida é que confere o caráter básico do acetaminofen.
III. A absorção do ácido acetilsalicílico em um indivíduo é maior no estômago do que no intestino, devido ao baixo pH do suco gástrico.
IV. Os fenóis apresentam menor acidez do que os ácidos carboxílicos.
São corretas as afirmações

Considere a figura com a estrutura do acetaminofen e as seguintes afirmações:
I. O acetaminofen apresenta fórmula molecular
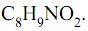
II. O grupo funcional amida é que confere o caráter básico do acetaminofen.
III. A absorção do ácido acetilsalicílico em um indivíduo é maior no estômago do que no intestino, devido ao baixo pH do suco gástrico.
IV. Os fenóis apresentam menor acidez do que os ácidos carboxílicos.
São corretas as afirmações
Ano: 2007
Banca:
VUNESP
Órgão:
UNIFESP
Prova:
VUNESP - 2007 - UNIFESP - Vestibular - Conhecimentos Gerais |
Q218451
Química
O nitrito de sódio, 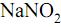 é um dos aditivos mais utilizados na conservação de alimentos. É um excelente agente antimicrobiano e está presente em quase todos os alimentos industrializados à base de carne, tais como presuntos, mortadelas, salames, entre outros. Alguns estudos indicam que a ingestão deste aditivo pode proporcionar a formação no estômago de ácido nitroso e este desencadear a formação de metabólitos carcinogênicos.
é um dos aditivos mais utilizados na conservação de alimentos. É um excelente agente antimicrobiano e está presente em quase todos os alimentos industrializados à base de carne, tais como presuntos, mortadelas, salames, entre outros. Alguns estudos indicam que a ingestão deste aditivo pode proporcionar a formação no estômago de ácido nitroso e este desencadear a formação de metabólitos carcinogênicos.
Dada a constante de hidrólise: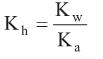
e considerando as constantes de equilíbrio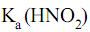 = 5 × 10–4 e
= 5 × 10–4 e 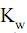 = 1 × 10–14, a 25 oC, o pH de uma solução aquosa de nitrito de sódio 5 × 10–2 mol/L nesta mesma temperatura tem valor aproximadamente igual a
= 1 × 10–14, a 25 oC, o pH de uma solução aquosa de nitrito de sódio 5 × 10–2 mol/L nesta mesma temperatura tem valor aproximadamente igual a
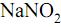 é um dos aditivos mais utilizados na conservação de alimentos. É um excelente agente antimicrobiano e está presente em quase todos os alimentos industrializados à base de carne, tais como presuntos, mortadelas, salames, entre outros. Alguns estudos indicam que a ingestão deste aditivo pode proporcionar a formação no estômago de ácido nitroso e este desencadear a formação de metabólitos carcinogênicos.
é um dos aditivos mais utilizados na conservação de alimentos. É um excelente agente antimicrobiano e está presente em quase todos os alimentos industrializados à base de carne, tais como presuntos, mortadelas, salames, entre outros. Alguns estudos indicam que a ingestão deste aditivo pode proporcionar a formação no estômago de ácido nitroso e este desencadear a formação de metabólitos carcinogênicos.Dada a constante de hidrólise:
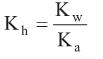
e considerando as constantes de equilíbrio
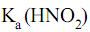 = 5 × 10–4 e
= 5 × 10–4 e 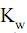 = 1 × 10–14, a 25 oC, o pH de uma solução aquosa de nitrito de sódio 5 × 10–2 mol/L nesta mesma temperatura tem valor aproximadamente igual a
= 1 × 10–14, a 25 oC, o pH de uma solução aquosa de nitrito de sódio 5 × 10–2 mol/L nesta mesma temperatura tem valor aproximadamente igual a