Questões de Vestibular MACKENZIE 2010 para Vestibular
Foram encontradas 2 questões
Ano: 2010
Banca:
Universidade Presbiteriana Mackenzie
Órgão:
MACKENZIE
Prova:
Universidade Presbiteriana Mackenzie - 2010 - MACKENZIE - Vestibular |
Q1336297
Química
A GÊNESE DAS BOLHAS
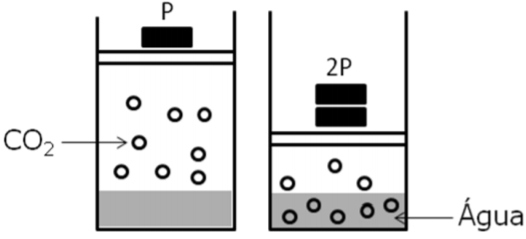
No champanhe, nos vinhos espumantes e nas cervejas, o dióxido de carbono (CO2) é o principal responsável pela formação das bolhas, originadas quando o levedo fermenta os açúcares, convertendo-os em moléculas de álcool e de CO2.
Após o engarrafamento, é estabelecido um equilíbrio entre o gás carbônico dissolvido no líquido e o gás que está no espaço sob a rolha ou a tampa.
Considerando as informações do texto, os seus conhecimentos químicos e a figura dada, é INCORRETO afirmar que

No champanhe, nos vinhos espumantes e nas cervejas, o dióxido de carbono (CO2) é o principal responsável pela formação das bolhas, originadas quando o levedo fermenta os açúcares, convertendo-os em moléculas de álcool e de CO2.
Após o engarrafamento, é estabelecido um equilíbrio entre o gás carbônico dissolvido no líquido e o gás que está no espaço sob a rolha ou a tampa.
Considerando as informações do texto, os seus conhecimentos químicos e a figura dada, é INCORRETO afirmar que
Ano: 2010
Banca:
Universidade Presbiteriana Mackenzie
Órgão:
MACKENZIE
Prova:
Universidade Presbiteriana Mackenzie - 2010 - MACKENZIE - Vestibular |
Q1336299
Química
O processo de Haber-Bosch para obtenção de amônia recebeu esse nome devido
aos seus criadores: Fritz Haber (1868 – 1934) e William Carl Bosch (1874 –
1940). Foi usado pela primeira vez, em escala industrial, na Alemanha, durante
a Primeira Guerra Mundial, com o objetivo de obtenção de matéria-prima para
produção de explosivos, associado ao processo Ostwald. A equação termoquímica
do processo Haber-Bosch é abaixo apresentada.
N2(g) + 3 H2(g) 2 NH3(g) ∆H = - 92,22 kJ
2 NH3(g) ∆H = - 92,22 kJ
Com o intuito de favorecer a produção de amônia, foram feitas, no sistema, as intervenções de I a V.
I. Aumento da pressão total do sistema.
II. Aumento da pressão parcial do gás amônia.
III. Diminuição da concentração do gás hidrogênio.
IV. Aumento da concentração do gás nitrogênio.
V. Utilização de um catalisador de ferro metálico.
São eficientes, para esse propósito, apenas as intervenções
N2(g) + 3 H2(g)
Com o intuito de favorecer a produção de amônia, foram feitas, no sistema, as intervenções de I a V.
I. Aumento da pressão total do sistema.
II. Aumento da pressão parcial do gás amônia.
III. Diminuição da concentração do gás hidrogênio.
IV. Aumento da concentração do gás nitrogênio.
V. Utilização de um catalisador de ferro metálico.
São eficientes, para esse propósito, apenas as intervenções