Questões de Vestibular UFVJM-MG 2018 para Vestibular - 2º Etapa
Foram encontradas 3 questões
Ano: 2018
Banca:
UFVJM-MG
Órgão:
UFVJM-MG
Prova:
UFVJM-MG - 2018 - UFVJM-MG - Vestibular - 2º Etapa |
Q1274494
Química
Denomina-se difusão gasosa espalhamento de um gás em outro meio gasoso. Graham, ao estudar esse
fenômeno, concluiu que, nas mesmas condições, as velocidades (v) de difusão de dois gases são
inversamente proporcionais às raízes quadradas de suas densidades absolutas (d) ou massas molares (M),
ou seja:
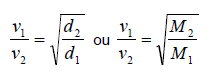
Em um laboratório, um observador estava à mesma distância de dois frascos idênticos: o primeiro continha metano (CH4) enquanto que o segundo continha metil-amina (CH3-NH2), ambos com cheiros característicos. Quando os frascos forem quebrados no mesmo momento o observador sentirá primeiro o cheiro de:
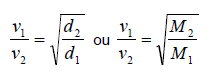
Em um laboratório, um observador estava à mesma distância de dois frascos idênticos: o primeiro continha metano (CH4) enquanto que o segundo continha metil-amina (CH3-NH2), ambos com cheiros característicos. Quando os frascos forem quebrados no mesmo momento o observador sentirá primeiro o cheiro de:
Ano: 2018
Banca:
UFVJM-MG
Órgão:
UFVJM-MG
Prova:
UFVJM-MG - 2018 - UFVJM-MG - Vestibular - 2º Etapa |
Q1274495
Química
O carbonato de cálcio (CaCO3) é, recentemente, um dos principais compostos pesquisados na área de
materiais, sobretudo em cerâmicas, como na produção de tijolos. Uma das maneiras de produção do
CaCO3 é pela reação entre o hidróxido de cálcio, Ca(OH)2, e de ácido carbônico, H2CO3 conforme esta
equação:
H2CO3(aq) + Ca(OH)2(aq) → CaCO3(s) + 2 H2O(l) Equação 1
São apresentadas as entalpias-padrão de reação, em kJmol-1 , para três reações a 25ºC:
I - CaO(s) + CO2(g) → CaCO3 (s) ΔHº = -183,3 kJmol-1 Equação 2 II - CaO (s) + H2O(l) → Ca(OH)2(aq) ΔHº = - 82,4 kJmol-1 Equação 3 III - CO2(g) + H2O(l) → H2CO3(aq) ΔHº = - 20,5 kJmol-1 Equação 4
O valor da entalpia-padrão, em kJ, para a produção do carbonato na reação da equação 1 é:
H2CO3(aq) + Ca(OH)2(aq) → CaCO3(s) + 2 H2O(l) Equação 1
São apresentadas as entalpias-padrão de reação, em kJmol-1 , para três reações a 25ºC:
I - CaO(s) + CO2(g) → CaCO3 (s) ΔHº = -183,3 kJmol-1 Equação 2 II - CaO (s) + H2O(l) → Ca(OH)2(aq) ΔHº = - 82,4 kJmol-1 Equação 3 III - CO2(g) + H2O(l) → H2CO3(aq) ΔHº = - 20,5 kJmol-1 Equação 4
O valor da entalpia-padrão, em kJ, para a produção do carbonato na reação da equação 1 é:
Ano: 2018
Banca:
UFVJM-MG
Órgão:
UFVJM-MG
Prova:
UFVJM-MG - 2018 - UFVJM-MG - Vestibular - 2º Etapa |
Q1274502
Química
O diamante é reconhecido mundialmente por sua rara beleza e brilho ofuscante. A lapidação do cristal tem
por objetivo realçar o brilho, criando facetas com ângulos e dimensões que permitem que a luz recebida
pela parte superior do cristal, por exemplo, seja refletida em seu interior e saia principalmente pela parte
superior. Desta forma, há o máximo de cintilação e de espalhamento da luz.
Um joalheiro bastante experiente lapidou um pedaço de vidro e um diamante do mesmo tamanho, cortando-os em inúmeras facetas e, a seguir, os poliu de forma a ficarem idênticos. Contudo, o vidro não apresenta o mesmo brilho do diamante ao ser incidido pela luz.
Fonte: SOUZA, Líria Alves de. "Brilho do diamante"; Brasil Escola. Disponível em <https://brasilescola.uol.com.br/quimica/brilho-diamante.htm>. Acesso em 20 de maio de 2018. (adaptado)
O vidro, mesmo após todo esse processo, não exibe o mesmo brilho pois o diamante é um sólido
Um joalheiro bastante experiente lapidou um pedaço de vidro e um diamante do mesmo tamanho, cortando-os em inúmeras facetas e, a seguir, os poliu de forma a ficarem idênticos. Contudo, o vidro não apresenta o mesmo brilho do diamante ao ser incidido pela luz.
Fonte: SOUZA, Líria Alves de. "Brilho do diamante"; Brasil Escola. Disponível em <https://brasilescola.uol.com.br/quimica/brilho-diamante.htm>. Acesso em 20 de maio de 2018. (adaptado)
O vidro, mesmo após todo esse processo, não exibe o mesmo brilho pois o diamante é um sólido