Questões de Vestibular UFRGS 2019 para Vestibular - UFRGS - Biologia, Química e Geografia
Foram encontradas 25 questões
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784284
Química
Na reação de cloração do 2-metilbutano em presença de luz ultravioleta, há formação de produtos
monossubstituídos e HCI. O número de produto(s) monossubstituído(s) diferente(s) que podem ser
formados é igual a
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784285
Química
A dessalinização da água do mar é um processo que transforma água do mar em água potável e
garante o abastecimento de milhões de pessoas no mundo. Abaixo são descritas algumas técnicas
empregadas nesse processo.
1 - Aquecimento da água do mar, seguido de evaporação e condensação do vapor d' água. 2 - Resfriamento da água do mar até formação de gelo, composto essencialmente de água pura. 3 - Passagem da água do mar por uma membrana semipermeável, através da aplicação de uma pressão elevada.
As propriedades coligativas, envolvidas nas técnicas descritas nos itens 1, 2 e 3, podem ser classificadas, respectivamente, como
1 - Aquecimento da água do mar, seguido de evaporação e condensação do vapor d' água. 2 - Resfriamento da água do mar até formação de gelo, composto essencialmente de água pura. 3 - Passagem da água do mar por uma membrana semipermeável, através da aplicação de uma pressão elevada.
As propriedades coligativas, envolvidas nas técnicas descritas nos itens 1, 2 e 3, podem ser classificadas, respectivamente, como
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784286
Química
Uma suspensão de sulfato de bário pode ser usada como agente de contraste em exames de raios-X. O
sulfato de bário é um sal pouco solúvel, com constante do produto de solubilidade 1,1 x 10-10•
Em relação a uma solução aquosa saturada desse sal, contendo uma certa quantidade de sal sólido, não dissolvido, são feitas as seguintes afirmações.
I - A adição de nitrato de bário diminui a quantidade de sólido não dissolvido. II - A adição de sulfato de sódio aumenta a quantidade de sólido não dissolvido. III - Uma reação reversível, na qual a dissolução do sal é exatamente contrabalançada pela sua precipitação, é estabelecida nessa situação.
Quais estão corretas?
Em relação a uma solução aquosa saturada desse sal, contendo uma certa quantidade de sal sólido, não dissolvido, são feitas as seguintes afirmações.
I - A adição de nitrato de bário diminui a quantidade de sólido não dissolvido. II - A adição de sulfato de sódio aumenta a quantidade de sólido não dissolvido. III - Uma reação reversível, na qual a dissolução do sal é exatamente contrabalançada pela sua precipitação, é estabelecida nessa situação.
Quais estão corretas?
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784287
Química
Uma solução é preparada misturando-se 40,00 ml de NaOH de concentração 0,30 mal L-1 e 60,00 ml
de KOH 0,20 mal L-1
•
As concentrações molares de íons Na+, K+ e OH- na solução resultante serão, em mal L-1 , respectivamente,
As concentrações molares de íons Na+, K+ e OH- na solução resultante serão, em mal L-1 , respectivamente,
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784288
Química
A reação de formação do etanol é definida abaixo.
2 C (s) + 3 H2 (g) + ½ 02 (g) --+ C2HsOH (1)
Embora essa reação, tal como está escrita, não possa ser realizada em laboratório, pode-se calcular seu efeito térmico, mediante uma combinação adequada de outras reações.
Usando as reações abaixo,
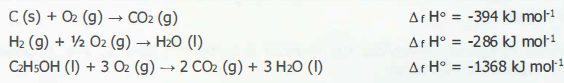
a entalpia da reação de formação do etanol, em kJ mo1-1 , é
2 C (s) + 3 H2 (g) + ½ 02 (g) --+ C2HsOH (1)
Embora essa reação, tal como está escrita, não possa ser realizada em laboratório, pode-se calcular seu efeito térmico, mediante uma combinação adequada de outras reações.
Usando as reações abaixo,
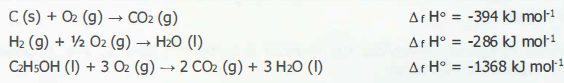
a entalpia da reação de formação do etanol, em kJ mo1-1 , é
