Questões de Vestibular UERJ 2015 para Vestibular - Primeiro Exame
Foram encontradas 4 questões
O suco gástrico contém um ácido, produzido pelas células da parede do estômago, que desempenha papel fundamental para a eficiência do processo digestório no ser humano.
O ânion do ácido produzido no estômago corresponde ao elemento químico pertencente ao grupo 17 e ao terceiro período da tabela de classificação periódica.
Esse ácido é denominado:
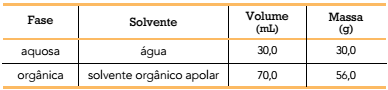
Para diferenciar as duas fases, originariamente incolores, é adicionado ao óleo um corante azul de natureza iônica, que se dissolve apenas na fase em que o solvente apresenta maior afinidade pelo corante. Essa adição não altera as massas e volumes das fases líquidas.
As duas fases líquidas do óleo bifásico podem ser representadas pelo seguinte esquema:
Em um experimento, foi analisado o efeito do número de átomos de carbono sobre a solubilidade de alcoóis em água, bem como sobre a quiralidade das moléculas desses alcoóis. Todas as moléculas de alcoóis testadas tinham número de átomos de carbono variando de 2 a 5, e cadeias carbônicas abertas e não ramificadas.
Dentre os alcoóis utilizados contendo um centro quiral, aquele de maior solubilidade em água possui fórmula estrutural correspondente a:
2 NaHCO3 (s) → Na2CO3 (s) + H 2O (g) + CO2 (g)
Considere o preparo de dois bolos com as mesmas quantidades de ingredientes e sob as mesmas condições, diferindo apenas na temperatura do forno: um foi cozido a 160 oC e o outro a 220 oC. Em ambos, todo o fermento foi consumido.
O gráfico que relaciona a massa de CO2 formada em função do tempo de cozimento, em cada uma dessas temperaturas de preparo, está apresentado em: