Questões de Vestibular UDESC 2018 para Vestibular - Segundo Semestre (Tarde)
Foram encontradas 2 questões
A nitroglicerina - C3H5(NO3)3 – é um nitrato de alquila, descoberta em 1847 por Ascanio Sobrero (químico italiano, 1812-1888), que a obteve misturando glicerina, ácido nítrico e ácido sulfúrico. No estado puro e à temperatura ambiente, a nitroglicerina é um líquido muito explosivo e perigoso. Em 1867, Alfred Nobel (químico sueco, 1833-1896) realizou testes no sentido de melhorar a manipulação da nitroglicerina, misturando-a com materiais inertes, como sílica, pós cerâmicos, argila, gesso, carvão e terras diatomáceas. Esses materiais, agora moldáveis, viriam a se tornar um explosivo muito importante, conhecido como dinamite.
A equação abaixo (não balanceada) representa a reação de decomposição da nitroglicerina:
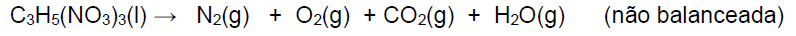
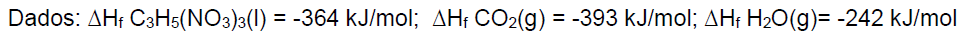
De posse das informações, assinale a alternativa que representa a variação de entalpia da
reação acima, em kJ por mol de nitroglicerina.
Um aluno mergulhou uma bobina de cobre (6,00 g) em uma solução de nitrato de prata (2,0 g dissolvidos em solução aquosa para 50 mL de volume total). Ele observou, após a ocorrência da reação, a deposição de um sólido acinzentado sobre a bobina de cobre, e também notou que a solução adquiriu uma coloração azul. A massa do sólido cinza foi de 1,2 g e a massa da bobina 5,50 g. As equações abaixo podem ser utilizadas para descrever a reação que ocorre no experimento:
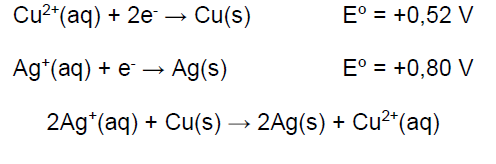
Analise as proposições em relação às informações e às equações acima.
I. A concentração da solução de nitrato de prata é 0,2 mol/L
II. Essa reação pode ser considerada uma pilha com um ΔEº = 0,28 V.
III. A prata oxida nessa reação.
IV. O sólido que se deposita sobre a bobina de cobre é de prata metálica.
V. O cobre é o agente redutor, sofrendo redução.
VI. A quantidade de prata produzida (sólido cinza) foi de 0,011 mol e a quantidade de cobre consumida 0,0079 mol.
Assinale a alternativa correta.