Questões de Vestibular UDESC 2018 para Vestibular - Física \ Química \ História \ Geografia
Foram encontradas 14 questões

Em
um estudo recente, pesquisadores brasileiros realizaram a avaliação ambiental
de BTEX (benzeno, tolueno, etilbenzeno e xilenos) e biomarcadores de
genotoxicidade em trabalhadores de postos de combustíveis. Após as análises,
concluiu-se que as concentrações de BTEX estavam dentro dos valores
preconizados pela legislação vigente. No entanto, o estudo sugeriu, também, que
a exposição ao BTEX, mesmo em baixas concentrações, contribui para o risco
genotóxico à saúde humana.
A
seguir são apresentadas quatro estruturas químicas presentes no BTEX:
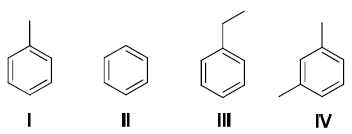
Assinale a alternativa que contém os nomes das estruturas químicas apresentadas acima, respectivamente.

O elemento químico X possui 15 nêutrons, é isótopo do elemento químico Y, que possui 13 prótons, e isóbaro do elemento químico Z, que tem 12 nêutrons.
Com base nessas informações, pode-se afirmar que os elementos químicos X, Y e Z apresentam, respectivamente, números atômicos iguais a:
São chamadas de funções químicas os grupos de substâncias que apresentam propriedades químicas e comportamentos semelhantes. Na química orgânica, as chamadas 'funções orgânicas" são os compostos que têm comportamento químico similar devido à presença de um grupo funcional característico. São exemplos de funções orgânicas: álcoois, ésteres, éteres, amidas, aminas e ácidos carboxílicos.
Assinale a alternativa que contém os compostos que fazem parte das funções éster, amina e respectivamente.
respectivamente.

Quando se balancear uma reação química, deve-se obedecer à lei da conservação da massa. Ao se balancear reações de oxirredução, existe uma exigência adicional: os elétrons recebidos e doados devem estar balanceados.
Desta forma, é correto afirmar que a reação de oxirredução entre o íon permanganato e o íon oxalato em solução aquosa ácida, representada abaixo, estará balanceada quando os coeficientes estequiométricos forem, respectivamente:
MnO4- (aq) + C2O42- (aq) + H+ (aq) Mn2+ (aq) + H2O (l) + CO2 (g)
Mn2+ (aq) + H2O (l) + CO2 (g)