Questões de Vestibular PUC - RJ 2018 para Vestibular - 1° Dia , Grupo 1 - Tarde
Foram encontradas 10 questões
Ano: 2018
Banca:
PUC - RJ
Órgão:
PUC - RJ
Provas:
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 1 - Tarde
|
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 2 - Tarde |
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 4 - Tarde |
Q1261990
Química
O ácido clorídrico (HCl) é um ácido inorgânico forte. Na coluna da esquerda são listados compostos que reagem
com solução concentrada de ácido clorídrico e na coluna da direita, indícios de que houve reação.
( ) CaCO3(aq) ( ) NaOH(aq) diluído na presença de fenolftaleína ( ) limalha fina de Zn(s)
1 – mudança de cor 2 – formação de gás 3 – desaparecimento do material sólido 4 – formação de precipitado
Associando a coluna da direita com a da esquerda, a sequência correta de números é
( ) CaCO3(aq) ( ) NaOH(aq) diluído na presença de fenolftaleína ( ) limalha fina de Zn(s)
1 – mudança de cor 2 – formação de gás 3 – desaparecimento do material sólido 4 – formação de precipitado
Associando a coluna da direita com a da esquerda, a sequência correta de números é
Ano: 2018
Banca:
PUC - RJ
Órgão:
PUC - RJ
Provas:
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 1 - Tarde
|
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 2 - Tarde |
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 4 - Tarde |
Q1261991
Química
O nióbio é um metal usado para produção de ligas especiais. Ele é obtido a partir da redução do pentóxido de
nióbio na presença de alumínio e óxido de ferro (III), como mostrado na equação química a seguir:
3 Nb2O5 (s) + Fe2O3 (s) + 12 Al (s) → 6 Nb (s) + 2 Fe (s) + 6 Al2O3 (s)
Assumindo o rendimento completo da reação, a massa mais próxima de nióbio metálico, em kg, que seria obtida a partir de 850 kg de Nb2O5 é:
Dados: M (Nb) = 93 g mol-1 M (Nb2O5) = 266 g mol-1
3 Nb2O5 (s) + Fe2O3 (s) + 12 Al (s) → 6 Nb (s) + 2 Fe (s) + 6 Al2O3 (s)
Assumindo o rendimento completo da reação, a massa mais próxima de nióbio metálico, em kg, que seria obtida a partir de 850 kg de Nb2O5 é:
Dados: M (Nb) = 93 g mol-1 M (Nb2O5) = 266 g mol-1
Ano: 2018
Banca:
PUC - RJ
Órgão:
PUC - RJ
Provas:
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 1 - Tarde
|
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 2 - Tarde |
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 4 - Tarde |
Q1261992
Química
O arranjo dos átomos numa estrutura molecular ou iônica varia em função do número e do tamanho relativo dos
átomos envolvidos, da presença de elétrons não ligantes e do tipo de ligação entre os átomos. As espécies químicas
que têm, na ordem indicada, geometrias moleculares, trigonal plana, linear, angular e tetraédrica, são
Ano: 2018
Banca:
PUC - RJ
Órgão:
PUC - RJ
Provas:
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 1 - Tarde
|
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 2 - Tarde |
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 4 - Tarde |
Q1261995
Química
Uma massa de 10,40 g de cloreto de bário (BaCl2) foi pesada em balança e depois totalmente dissolvida, formando
500,00 mL de solução aquosa. Dessa solução, transferiu-se uma alíquota de 100,00 mL para um balão volumétrico
de 250,00 mL, que teve volume ajustado com água pura. O valor que mais se aproxima da concentração de Ba2+
,
em mol L-1
, na solução contida no balão volumétrico de 250,00 mL, é o seguinte
Dado: M (BaCl2) = 208,0 g mol-1
Dado: M (BaCl2) = 208,0 g mol-1
Ano: 2018
Banca:
PUC - RJ
Órgão:
PUC - RJ
Provas:
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 1 - Tarde
|
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 2 - Tarde |
PUC - RJ - 2018 - PUC - RJ - Vestibular - 1° Dia - Grupo 4 - Tarde |
Q1261996
Química
Considere uma solução aquosa na qual se tem o equilíbrio abaixo.
NH4OH(aq)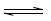 NH4+(aq) + OH-
(aq)
NH4+(aq) + OH-
(aq)
Adiciona-se 1 mL de solução aquosa de cloreto de amônio (NH4Cl),com concentração igual a 1 mol L-1 , a 100 mL da solução aquosa de concentração igual a 0,1 mol L -1 de hidróxido de amônio (NH4OH). Após a adição da solução salina, o pH da solução resultante, em relação ao pH da solução original de NH4OH, se torna
NH4OH(aq)
 NH4+(aq) + OH-
(aq)
NH4+(aq) + OH-
(aq)
Adiciona-se 1 mL de solução aquosa de cloreto de amônio (NH4Cl),com concentração igual a 1 mol L-1 , a 100 mL da solução aquosa de concentração igual a 0,1 mol L -1 de hidróxido de amônio (NH4OH). Após a adição da solução salina, o pH da solução resultante, em relação ao pH da solução original de NH4OH, se torna