Questões de Vestibular PUC - RJ 2014 para Vestibular , 2° Dia Prova Tarde grupo 3
Foram encontradas 9 questões
I. KCl(aq) + AgNO3(aq) → AgCl(s) + KNO3(aq)
II. FeCl3(aq) + SnCl2(aq) → FeCl2(aq) + SnCl4(aq)
III. Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + H2O(l)
Nessas equações, os símbolos (aq), (s) e (l) representam, respectivamente, “espécies químicas dissolvidas em água", “espécies químicas no estado sólido" e “espécies químicas no estado líquido".
É correto afirmar que, na reação indicada, são íons espectadores
Num processo de fissão nuclear, um nêutron colidiu com o núcleo de um isótopo do urânio levando à formação de dois núcleos menores e liberação de nêutrons que produziram reações em cadeia com liberação de grande quantidade de energia. Uma das possíveis reações nucleares nesse processo é representada por:
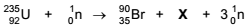
O produto X, formado na fissão nuclear indicada acima, é
um isótopo do elemento químico:
Considere: R = 0,082 atm L mol-1 K-1
M(O2) = 32 g mol-1
Considere: M(Cu) = 63,5 g mol-1
M(S) = 32 g mol-1