Questões de Vestibular PUC - Campinas 2015 para Vestibular
Foram encontradas 6 questões
O mineral calcita, CaCO3, é um dos principais constituintes do mármore. Esse mineral pode ser dissolvido com ácidos, porque ocorre a seguinte reação:
CaCO3 (s) + 2H+ (aq) → Ca2+ (aq) + CO2 (g) + H2O (l)
Considerando uma solução de ácido clorídrico cujo pH = 0, o volume dessa solução, em mL, necessário para dissolver 1,0 g de CaCO3 é deMassa molar do CaCO3 = 100 g.mol−1
A bomba atômica, também chamada de bomba nuclear,
tem como constituinte físsil átomos de urânio-235, 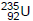 ,
emissores de partículas alfa
,
emissores de partículas alfa 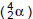 . Cada átomo de U-235,
ao emitir uma partícula alfa, transforma-se em outro
elemento, cujo número atômico é igual a
. Cada átomo de U-235,
ao emitir uma partícula alfa, transforma-se em outro
elemento, cujo número atômico é igual a
Um dos álcoois mais comuns, o etanol, queima completamente segundo a reação
C2H6O (l) + 3O2 (g) → 2CO2 (g) + 3H2O (g)
Considerando que todos os produtos dessa reação são gasosos, o volume de gás total, em m3 , produzido quando é queimado 1,0 kg de etanol, nas CNTP, é de, aproximadamente,
Dados:
Massas molares (g.mol−1 )
H = 1,0
C = 12,0
O = 16,0
Volume molar, nas CNTP = 22,4 L.mol−1
Quando um frasco cheio até a borda com um líquido é aquecido, em geral o líquido transborda devido à expansão de volume chamada de dilatação térmica.
Um cientista aquece o conjunto formado por um frasco de vidro cheio até a borda com um líquido, e observa que o nível do líquido abaixou.
Considerando que o frasco não possui nenhum furo ou rachadura e que a evaporação do líquido é desprezível, pode-se afirmar que
NH3 (g) + H2O ( l) ⇌ NH4 + (aq) + OH− (aq)
A liberação de gás amônia ocorrerá com maior intensidade quando a essa solução for adicionado
I. NH4Cl (aq).
II. FeCl3 (aq).
III. NaOH (aq).
Está correto o que consta APENAS em