Questões de Vestibular UFPR 2016 para Vestibular
Foram encontradas 9 questões
Q814922
Química
Folhas de repolho-roxo exibem cor intensa devido à presença de pigmentos. Processando-se algumas folhas num
liquidificador com um pouco de água, extrai-se um líquido de cor roxa, que, posteriormente, passa por uma peneira.
Foram realizados os seguintes experimentos, seguidos das observações:
• Sobre volume de meio copo (~100 mL) do extrato líquido, adicionaram-se 20 mL de solução salina de cloreto de sódio (1 mol L -1 ). A cor roxa do extrato foi mantida. • Sobre volume de meio copo do extrato líquido, adicionou-se suco de um limão. A cor do extrato líquido se tornou vermelha.
Foi observado aspecto opaco (turvo) no extrato líquido logo em seguida à sua separação das folhas de repolho, e esse aspecto se manteve durante todos os experimentos.
Sobre esse experimento, considere as seguintes afirmativas:
1. A mudança de cor de roxa para vermelha no segundo experimento é evidência de que ocorreu uma transformação química no extrato. 2. O extrato líquido é uma mistura homogênea. 3. Nos 20 mL de solução salina existem 1,2 x 1022 íons Na+ e 1,2 x 1022 íons Cl– .
Assinale a alternativa correta.
• Sobre volume de meio copo (~100 mL) do extrato líquido, adicionaram-se 20 mL de solução salina de cloreto de sódio (1 mol L -1 ). A cor roxa do extrato foi mantida. • Sobre volume de meio copo do extrato líquido, adicionou-se suco de um limão. A cor do extrato líquido se tornou vermelha.
Foi observado aspecto opaco (turvo) no extrato líquido logo em seguida à sua separação das folhas de repolho, e esse aspecto se manteve durante todos os experimentos.
Sobre esse experimento, considere as seguintes afirmativas:
1. A mudança de cor de roxa para vermelha no segundo experimento é evidência de que ocorreu uma transformação química no extrato. 2. O extrato líquido é uma mistura homogênea. 3. Nos 20 mL de solução salina existem 1,2 x 1022 íons Na+ e 1,2 x 1022 íons Cl– .
Assinale a alternativa correta.
Q814923
Química
As propriedades das substâncias químicas podem ser previstas a partir das configurações eletrônicas dos seus
elementos. De posse do número atômico, pode-se fazer a distribuição eletrônica e localizar a posição de um elemento
na tabela periódica, ou mesmo prever as configurações dos seus íons.
Sendo o cálcio pertencente ao grupo dos alcalinos terrosos e possuindo número atômico Z = 20, a configuração
eletrônica do seu cátion bivalente é:
Q814924
Química
A bauxita, constituída por uma mistura de óxidos, principalmente de alumínio (Al2O3) e ferro (Fe2O3 e Fe(OH)3), é o
principal minério utilizado para a produção de alumínio. Na purificação pelo processo Bayer, aproximadamente 3
toneladas de resíduo a ser descartado (lama vermelha) são produzidas a partir de 5 toneladas do minério. Com a
alumina purificada, alumínio metálico é produzido por eletrólise ígnea.
Dados – M (g mol-1 ): O = 16; Al = 27; Fe = 56.
A partir de 5 toneladas de minério, a quantidade (em toneladas) de alumínio metálico produzida por eletrólise ígnea é mais próxima de:
Dados – M (g mol-1 ): O = 16; Al = 27; Fe = 56.
A partir de 5 toneladas de minério, a quantidade (em toneladas) de alumínio metálico produzida por eletrólise ígnea é mais próxima de:
Q814925
Química
Em momentos de estresse, as glândulas suprarrenais secretam o hormônio
adrenalina, que, a partir da aceleração dos batimentos cardíacos, do aumento da
pressão arterial e da contração ou relaxamento de músculos, prepara o organismo
para a fuga ou para a defesa.
Dados – M (g mol-1 ): H = 1; C = 12; N = 14; O = 16.
Qual é o valor da massa molar (em g mol-1 ) desse composto?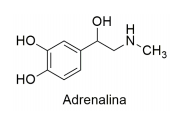
Dados – M (g mol-1 ): H = 1; C = 12; N = 14; O = 16.
Qual é o valor da massa molar (em g mol-1 ) desse composto?

Q814926
Química
Recentemente, foram realizados retratos genéticos e de habitat do mais antigo ancestral universal, conhecido como
LUCA. Acredita-se que esse organismo unicelular teria surgido a 3,8 bilhões de anos e seria capaz de fixar CO2,
convertendo esse composto inorgânico de carbono em compostos orgânicos.
Para converter o composto inorgânico de carbono mencionado em metano (CH4), a variação do NOX no carbono é de: