Questões de Vestibular UEL 2018 para Vestibular - 1º Fase
Foram encontradas 7 questões
O acetato de etila (CH3COOCH2CH3) é um éster simples, usado, no passado, como antiespasmódico e hoje como solvente industrial e removedor de esmalte de unha. A acetona (CH3(CO)CH3) também é usada como removedor de esmaltes, mas devido a sua elevada solubilidade em água, quando em contato com a pele, pode desidratá-la. Sabe-se que estes solventes possuem cheiros parecidos, tornando difícil a identificação pelo olfato.
Considerando um frasco contendo acetato de etila e acetona em quantidades equimolares, assinale a alternativa que apresenta, corretamente, o procedimento para a separação da mistura.
Dados:
Ponto de ebulição do acetato de etila a 1 atm =77,1 °C e densidade = 902 Kg/m3
Ponto de ebulição da acetona a 1 atm = 56,0 °C e densidade = 784 Kg/m3
Os cosméticos, como batons e rímeis, buscam realçar o encanto da beleza. Porém, o uso desses produtos pode, também, causar desencantamento em função dos constituintes químicos tóxicos que possuem. Em batons, pode haver presença de cádmio, chumbo, arsênio e alumínio. A FDA (Food and Drug Administration) e a ANVISA (Agência Nacional de Vigilância Sanitária) preconizam limites máximos de metais apenas para corantes orgânicos artificiais utilizados como matéria-prima na fabricação de cosméticos.
Considerando que um determinado batom possua concentração de chumbo igual a 1,0 mg Kg−1 e que a estimativa máxima de utilização deste cosmético ao longo do dia seja de 100 mg, assinale a alternativa que representa, correta e aproximadamente, o número de átomos de chumbo em contato com os lábios ao longo de um dia.
Dados:
Massa molar de chumbo = 207 g mol−1
Constante de Avogadro = 6,0 x 1023 mol−1
Em 2017, a ANVISA aprovou a administração de um medicamento antirretroviral composto pela combinação das substâncias entricitabina (FTC) e fumarato (molécula contendo ácido carboxílico como função orgânica) de tenofovir desoproxila (TDF) para pessoas com alto risco de infecção pelo vírus HIV. O medicamento apresenta Profilaxia Pré-Exposição (PrEP), ou seja, evita que uma pessoa que não tem HIV adquira a infecção quando se expõe ao vírus.
As estruturas químicas da FTC e do TDF são apresentada
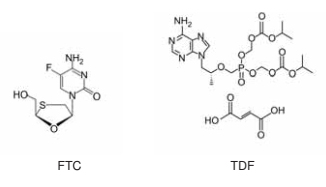
Dados:
Massa molar da FTC = 247,24 g mol−1
Massa molar do TDF = 635,52 g mol−1
Sabe-se que a solubilidade em água a 25 °C da FTC é 13,4 mg L−1 e do TDF é 112,0 mg mL−1 e que a constante de ionização da FTC é de 5,12 x 10−15, cujo hidrogênio ácido é aquele pertencente à hidroxila.
Com base nas estruturas químicas e nas informações apresentadas sobre as moléculas, assinale a alternativa
correta.
A hipoglicemia é caracterizada por uma concentração de glicose abaixo de 0,70 g L−1 no sangue. O quadro de hipoglicemia em situações extremas pode levar a crises convulsivas, perda de consciência e morte do indivíduo, se não for revertido a tempo. Entretanto, na maioria das vezes, o indivíduo, percebendo os sinais de hipoglicemia, consegue reverter este déficit, consumindo de 15 a 20 gramas de carboidratos, preferencialmente simples, como a glicose.
A metabolização da glicose, C6H12O6, durante a respiração, pode ser representada pela equação química de combustão:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l)
No quadro a seguir, são informadas reações químicas e seus respectivos calores de formação a 25 °C e 1 atm:

Sabendo que a Massa Molar (MM) da glicose é igual a 180,0 g mol−1, determine a quantidade aproximada de energia
liberada em kJ mol−1 no estado padrão, ΔHr°, na combustão da glicose, consumida em 350 mL de refrigerante
do tipo Cola, o qual possui, em sua composição, 35 g de glicose.
A contaminação de ecossistemas em função do crescimento populacional e da industrialização tem sido cada vez maior ao longo dos anos, mesmo com o advento de tecnologias voltadas à descontaminação ambiental. Um dos efeitos deletérios ao ambiente é a elevada acidez da chuva e de solos. A figura a seguir mostra o efeito que a acidez do solo causa na velocidade de lixiviação de íons Cd2+.
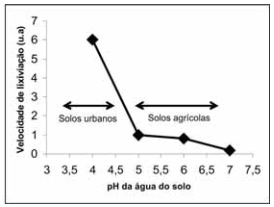
Dados: Kps para Cd(OH)2(s) = 2,5 x 10−14
Quanto maior a velocidade de lixiviação, maior o transporte de Cd2+ para os lagos por meio da corrente superficial ou subsuperficial, transferido para os aquíferos ou absorvido pela vegetação, com efeitos tóxicos.
Com base na figura e nos conhecimentos sobre solubilidade de metais e equilíbrio químico, é correto afirmar que
a lixiviação de cádmio