Questões de Vestibular UFT 2019 para Vestibular - Primeiro Semestre - Ciências Humanas e Ciências da Natureza
Foram encontradas 8 questões
Ano: 2019
Banca:
COPESE - UFT
Órgão:
UFT
Prova:
COPESE - UFT - 2019 - UFT - Vestibular - Primeiro Semestre - Ciências Humanas e Ciências da Natureza |
Q1399711
Química
A tabela apresenta as constantes físicas de alguns
cicloalcanos:
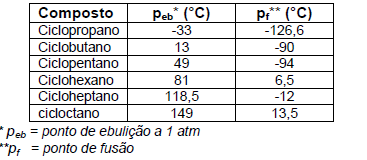
Com relação aos compostos apresentados na tabela, assinale a alternativa INCORRETA.

Com relação aos compostos apresentados na tabela, assinale a alternativa INCORRETA.
Ano: 2019
Banca:
COPESE - UFT
Órgão:
UFT
Prova:
COPESE - UFT - 2019 - UFT - Vestibular - Primeiro Semestre - Ciências Humanas e Ciências da Natureza |
Q1399712
Química
A quantidade de lixo eletrônico – resíduo de tecnologia como
circuitos impressos e telefones móveis – teve um crescimento
significativo na última década atingindo 40 milhões de
toneladas por ano mundialmente. Parte deste lixo eletrônico é
composto por metais preciosos (como o ouro), o que tem
levantando a possibilidade de reciclagem. Do total de lixo
eletrônico descartado, 30% é composto de metais e ligas
metálicas, sendo o restante composto por materiais não
metálicos e 300 ppm (partes por milhão) é composto por ouro.
Uma das propostas para recuperação do ouro descartado é o
tratamento com tiossulfato o qual apresenta elevada
especificidade para o ouro. A equação química da reação é
demonstrada a seguir. (Densidade dos materiais não metálicos
= 2,0 g/cm3
; massa molar do tiossulfato = 112 g.mol-1
, massa
molar do ouro = 196,97 g.mol-1
)
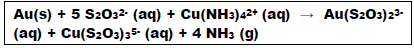
Analise as afirmativas em relação às informações:
I. Na reação demonstrada, o ouro é o agente redutor e o tiossulfato o agente oxidante.
II. É possível afirmar que são descartados anualmente 12 mil toneladas de ouro no lixo eletrônico.
III. A massa de material não metálico descartado anualmente é 1.000 vezes superior à massa de ouro descartada no mesmo período.
IV. Um volume de 14 milhões de metros cúbicos (m3 ) de materiais não metálicos são descartados anualmente no lixo eletrônico.
V. Seriam necessários 6,82 mil toneladas de tiossulfato para tratar a massa de ouro descartada no lixo eletrônico.
Assinale a alternativa CORRETA.

Analise as afirmativas em relação às informações:
I. Na reação demonstrada, o ouro é o agente redutor e o tiossulfato o agente oxidante.
II. É possível afirmar que são descartados anualmente 12 mil toneladas de ouro no lixo eletrônico.
III. A massa de material não metálico descartado anualmente é 1.000 vezes superior à massa de ouro descartada no mesmo período.
IV. Um volume de 14 milhões de metros cúbicos (m3 ) de materiais não metálicos são descartados anualmente no lixo eletrônico.
V. Seriam necessários 6,82 mil toneladas de tiossulfato para tratar a massa de ouro descartada no lixo eletrônico.
Assinale a alternativa CORRETA.
Ano: 2019
Banca:
COPESE - UFT
Órgão:
UFT
Prova:
COPESE - UFT - 2019 - UFT - Vestibular - Primeiro Semestre - Ciências Humanas e Ciências da Natureza |
Q1399713
Química
A química da origem da vida tem se revelado um desafio para
os cientistas. Embora experimentos como o de Miller-Urey
tenham sido capazes de produzir aminoácidos a partir de
compostos inorgânicos em condições específicas, estes
aminoácidos mostraram-se incapazes de produzir peptídeos
em meio aquoso nas condições utilizadas. Agora, um grupo de
pesquisadores foi capaz de sintetizar peptídeos diretamente de
compostos que poderiam ter existido na atmosfera primordial
da Terra. Matthew Powner, Pierre Canavelli e Saidul Islam
utilizaram aminonitrilas e compostos como gás sulfídrico e
ferrocianeto [ Fe(CN)6
3- ] para obter a ligação peptídica em
água. A síntese de peptídeos em meio aquoso mediada por
compostos de enxofre dá um passo adiante na pesquisa de
química pré-biótica.
Analise as afirmativas e assinale a alternativa CORRETA.
Analise as afirmativas e assinale a alternativa CORRETA.
Ano: 2019
Banca:
COPESE - UFT
Órgão:
UFT
Prova:
COPESE - UFT - 2019 - UFT - Vestibular - Primeiro Semestre - Ciências Humanas e Ciências da Natureza |
Q1399714
Química
A figura a seguir apresenta a tendência relativa de acidez de
alguns compostos químicos:
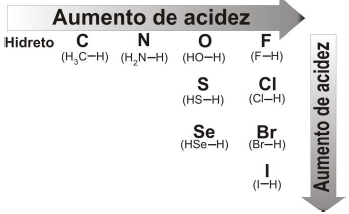
Analise os dados apresentados na figura e assinale a alternativa CORRETA.

Analise os dados apresentados na figura e assinale a alternativa CORRETA.
Ano: 2019
Banca:
COPESE - UFT
Órgão:
UFT
Prova:
COPESE - UFT - 2019 - UFT - Vestibular - Primeiro Semestre - Ciências Humanas e Ciências da Natureza |
Q1399715
Química
O peróxido de hidrogênio se decompõe lentamente segundo a
reação:
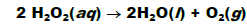
Na presença do íon brometo (Br- ), a decomposição ocorre rapidamente segundo as reações: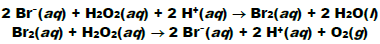
As reações vistas podem ser demonstradas graficamente a partir de um diagrama de energia potencial:
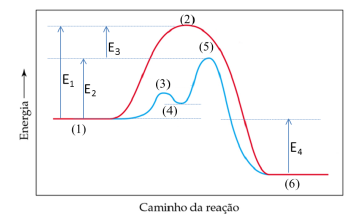
Em relação à decomposição do H2O2:
I. A reação sem catalisador acontece em apenas uma etapa e a reação com catalisador acontece em duas etapas, porém o produto formado é exatamente o mesmo.
II. E1 é a energia de ativação referente à decomposição do H2O2 na ausência de catalisador e E3 é a energia de ativação referente à decomposição do H2O2 na presença de catalisador. III. E2 é a energia de ativação da etapa determinante da velocidade da reação catalisada pelo íon Br- .
IV. E4 é a variação de entalpia da reação, que é endotérmica.
V. No gráfico, os pontos identificados por (2), (3) e (5) correspondem à energia dos complexos ativados para as reações representadas.
Assinale a alternativa CORRETA.
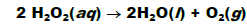
Na presença do íon brometo (Br- ), a decomposição ocorre rapidamente segundo as reações:
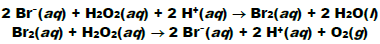
As reações vistas podem ser demonstradas graficamente a partir de um diagrama de energia potencial:

Em relação à decomposição do H2O2:
I. A reação sem catalisador acontece em apenas uma etapa e a reação com catalisador acontece em duas etapas, porém o produto formado é exatamente o mesmo.
II. E1 é a energia de ativação referente à decomposição do H2O2 na ausência de catalisador e E3 é a energia de ativação referente à decomposição do H2O2 na presença de catalisador. III. E2 é a energia de ativação da etapa determinante da velocidade da reação catalisada pelo íon Br- .
IV. E4 é a variação de entalpia da reação, que é endotérmica.
V. No gráfico, os pontos identificados por (2), (3) e (5) correspondem à energia dos complexos ativados para as reações representadas.
Assinale a alternativa CORRETA.