Questões de Vestibular UFT 2013 para Vestibular, Prova 02
Foram encontradas 40 questões
Q1263265
Química
Um aluno foi ao laboratório a fim de determinar o teor de ácido
acetilsalicílico (AAS) em um comprimido de aspirina.
Verificando que o melhor método seria a titulação indireta (por
retorno), pesou o comprimido (massa = 500 mg) e dissolveu
em um erlenmeyer, com a adição de 30 mL de hidróxido de
sódio, NaOH, a 0,5 mol/L. O excesso da base foi titulado com
ácido sulfúrico, H2SO4, a 0,5 mol/L, gastando 10 mL de ácido.
Sabendo que para cada mol de ácido acetilsalicílico são
consumidos dois mols de hidróxido de sódio, o teor de AAS na
amostra original é: (Dado: massa molar do AAS = 180 g/mol)
Q1263266
Química
No nosso dia-a-dia, convivemos com vários processos que são
denominados de fenômenos físicos e fenômenos químicos.
Fenômenos físicos são aqueles em que ocorrem mudanças de
fase da matéria sem alterar sua composição química. Já os
fenômenos químicos são aqueles que ocorrem com alteração
da composição química das substâncias. Qual das alternativas
a seguir contém somente fenômenos químicos?
Q1263267
Química
O ramo da Química que leva em consideração os aspectos
espaciais da estrutura molecular é chamado de
estereoquímica. Os enantiômeros são isômeros cujas
moléculas são imagens especulares não sobreponíveis entre
si. Sobre os enantiômeros é CORRETO afirmar:
Q1263268
Química
O Princípio de Le Chatelier diz que “Quando uma perturbação
exterior é aplicada a um sistema em equilíbrio dinâmico, ele
tende a ajustar para reduzir ao mínimo o efeito da
perturbação." Considere uma mistura de quatro gases, NH3,
O2, NO e H2O, colocada em um reator, atingindo o equilíbrio
conforme a reação
4NH3 (g) + 5O2 (g) 4NO (g) + 6H2O (g)
4NO (g) + 6H2O (g)  H < 0
H < 0
Qual das afirmações a seguir é INCORRETA?
4NH3 (g) + 5O2 (g)
 4NO (g) + 6H2O (g)
4NO (g) + 6H2O (g)  H < 0
H < 0 Qual das afirmações a seguir é INCORRETA?
Q1263269
Química
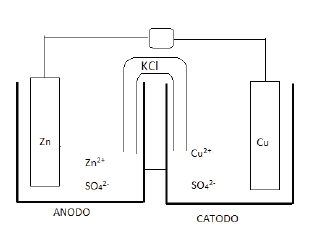
A figura a seguir representa uma célula galvânica conhecida
como a pilha de Daniell. No compartimento da esquerda, tem
uma placa de zinco mergulhada em solução de sulfato de zinco
a 1,00 mol/L e, no compartimento da direita, tem uma placa de
cobre mergulhada em uma solução de sulfato de cobre 1,00
mol/L. As placas estão interligadas por um fio condutor (circuito
externo) e as soluções estão unidas por uma ponte salina que
é uma solução saturada de cloreto de potássio. O potencial
padrão de redução do Zn2+ é -0,76V e do Cu2+ é +0,34V.
Analise as afirmações a seguir em relação ao funcionamento dessa pilha:
I. No anodo ocorre a oxidação do zinco e no catodo a redução do cobre. II. A carga do anodo é positiva e a do catodo negativa. III. O fluxo de elétrons ocorre do anodo para o catodo através do circuito externo. IV. Na placa de zinco, ocorre corrosão, liberando íons Zn2+ para a solução, enquanto que, na placa de cobre, ocorre deposição de Cu metálico. V. A função da ponte salina é balancear as cargas, sendo que os cátions K+ migram para a solução de sulfato de zinco e os ânions Cl- migram para a solução de sulfato de cobre. VI. O potencial padrão dessa pilha é 1,10 volts. VII. O Zn2+ é o agente oxidante e o Cu2+ é o agente redutor.
A alternativa que indica todas as afirmações CORRETAS é:

Analise as afirmações a seguir em relação ao funcionamento dessa pilha:
I. No anodo ocorre a oxidação do zinco e no catodo a redução do cobre. II. A carga do anodo é positiva e a do catodo negativa. III. O fluxo de elétrons ocorre do anodo para o catodo através do circuito externo. IV. Na placa de zinco, ocorre corrosão, liberando íons Zn2+ para a solução, enquanto que, na placa de cobre, ocorre deposição de Cu metálico. V. A função da ponte salina é balancear as cargas, sendo que os cátions K+ migram para a solução de sulfato de zinco e os ânions Cl- migram para a solução de sulfato de cobre. VI. O potencial padrão dessa pilha é 1,10 volts. VII. O Zn2+ é o agente oxidante e o Cu2+ é o agente redutor.
A alternativa que indica todas as afirmações CORRETAS é: