Questões de Vestibular UFSC 2010 para Vestibular, Prova 2
Foram encontradas 14 questões
O medicamento utilizado para destacar órgãos em exames radiológicos pode ter causado a morte de pelo menos 21 pessoas no país. Sua matéria-prima é o sulfato de bário. Análise preliminar da Fiocruz (Fundação Oswaldo Cruz) apontou a presença de carbonato de bário em um lote do produto distribuído por determinado laboratório. O carbonato de bário é utilizado em venenos para rato. Pacientes tomam sulfato de bário para que os órgãos de seu sistema digestório fiquem visíveis nas radiografias. É o chamado contraste.
Considere que o Ks do sulfato de bário é 1 x 10-10 .
O sulfato de bário é administrado na forma de uma suspensão.
Disponível em: <http://www1.folha.uol.com.br/folha/cotidiano/ult95u76538.shtml> Acesso em: 10 ago. 2010. (Adaptado)
Sobre o assunto, assinale a proposição CORRETA.
Na reação de sulfato de bário com HCl ocorre a formação de CO2, água e cloreto de bário.
O medicamento utilizado para destacar órgãos em exames radiológicos pode ter causado a morte de pelo menos 21 pessoas no país. Sua matéria-prima é o sulfato de bário. Análise preliminar da Fiocruz (Fundação Oswaldo Cruz) apontou a presença de carbonato de bário em um lote do produto distribuído por determinado laboratório. O carbonato de bário é utilizado em venenos para rato. Pacientes tomam sulfato de bário para que os órgãos de seu sistema digestório fiquem visíveis nas radiografias. É o chamado contraste.
Considere que o Ks do sulfato de bário é 1 x 10-10 .
O sulfato de bário é administrado na forma de uma suspensão.
Disponível em: <http://www1.folha.uol.com.br/folha/cotidiano/ult95u76538.shtml> Acesso em: 10 ago. 2010. (Adaptado)
Sobre o assunto, assinale a proposição CORRETA.
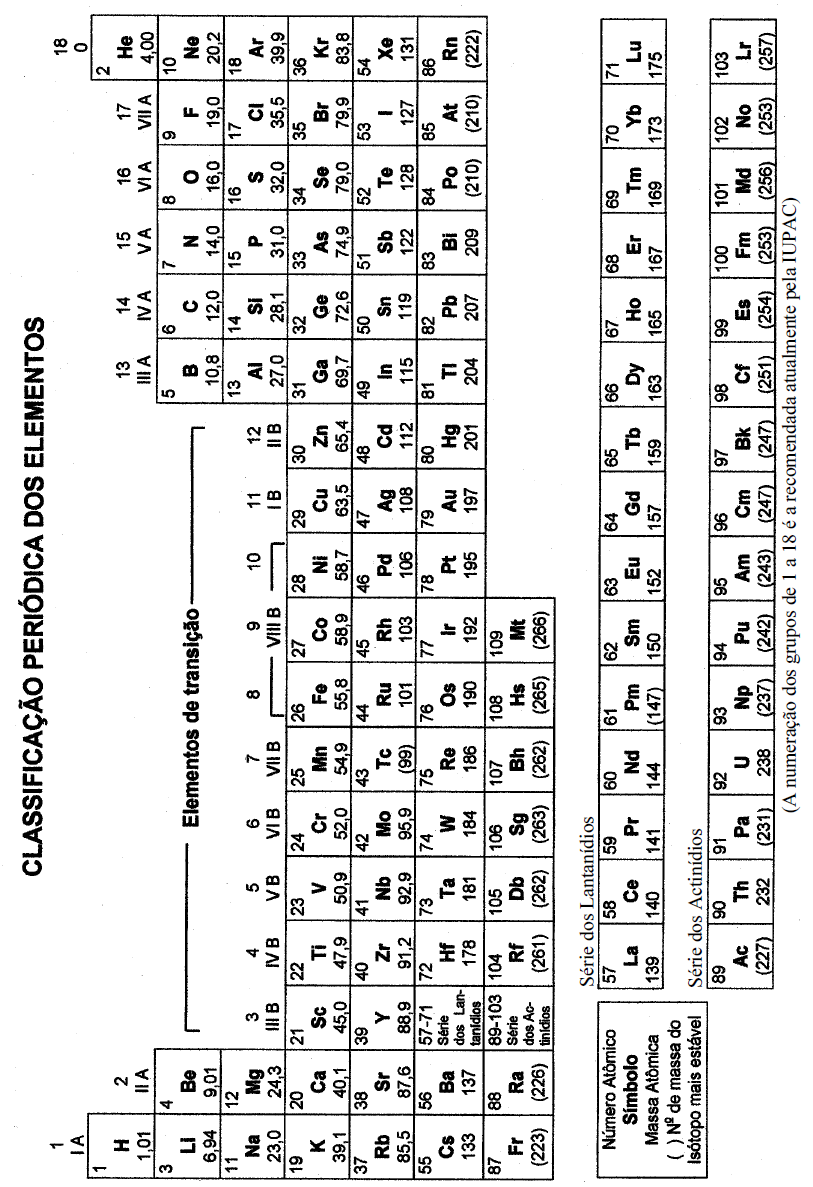
O raio atômico do bário é menor que o raio atômico do cálcio.
O medicamento utilizado para destacar órgãos em exames radiológicos pode ter causado a morte de pelo menos 21 pessoas no país. Sua matéria-prima é o sulfato de bário. Análise preliminar da Fiocruz (Fundação Oswaldo Cruz) apontou a presença de carbonato de bário em um lote do produto distribuído por determinado laboratório. O carbonato de bário é utilizado em venenos para rato. Pacientes tomam sulfato de bário para que os órgãos de seu sistema digestório fiquem visíveis nas radiografias. É o chamado contraste.
Considere que o Ks do sulfato de bário é 1 x 10-10 .
O sulfato de bário é administrado na forma de uma suspensão.
Disponível em: <http://www1.folha.uol.com.br/folha/cotidiano/ult95u76538.shtml> Acesso em: 10 ago. 2010. (Adaptado)
Sobre o assunto, assinale a proposição CORRETA.
O potencial de ionização do bário é maior que o potencial de ionização do sódio.
O medicamento utilizado para destacar órgãos em exames radiológicos pode ter causado a morte de pelo menos 21 pessoas no país. Sua matéria-prima é o sulfato de bário. Análise preliminar da Fiocruz (Fundação Oswaldo Cruz) apontou a presença de carbonato de bário em um lote do produto distribuído por determinado laboratório. O carbonato de bário é utilizado em venenos para rato. Pacientes tomam sulfato de bário para que os órgãos de seu sistema digestório fiquem visíveis nas radiografias. É o chamado contraste.
Considere que o Ks do sulfato de bário é 1 x 10-10 .
O sulfato de bário é administrado na forma de uma suspensão.
Disponível em: <http://www1.folha.uol.com.br/folha/cotidiano/ult95u76538.shtml> Acesso em: 10 ago. 2010. (Adaptado)
Sobre o assunto, assinale a proposição CORRETA.
A eletronegatividade do bário é maior que a do cobre.
Em uma indústria do Estado de São Paulo que produz ácido sulfúrico 98% a partir da queima de enxofre elementar, com capacidade de produção inicial de 600 toneladas por dia, ocorreu uma emissão de gás dióxido de enxofre (SO2). Essa emissão de gás ultrapassou as fronteiras da fábrica de ácido sulfúrico e atingiu a população do entorno. Várias pessoas apresentaram agravos à saúde relacionados ao caso, como irritação das vias aéreas, desmaios, vômitos e enjoos, demandando atendimento hospitalar de emergência em hospitais da região. Também foram acionados o Serviço de Atendimento Médico de Urgência (SAMU) e o Corpo de Bombeiros.
JÚNIOR, L.M.; LORENZI, R.L. Revista brasileira de saúde ocupacional. São Paulo: 32(116): 31-37, 2007. (Adaptado)
Sobre o assunto, é CORRETO afirmar que:
a queima do enxofre elementar pode ser representada pela equação química: S + O2 → SO2.