Questões de Vestibular CESMAC 2018 para Vestibular Medicina - Dia 2
Foram encontradas 60 questões
Q1797129
Química
O vanádio, na forma de pó metálico, pode causar mal-estar, entre outros sintomas. Além disso, a exposição
prolongada ao vanádio pode deixar a língua da pessoa
contaminada com a cor azul. Com relação ao vanádio,
na sua forma elementar, sua distribuição eletrônica nos
orbitais atômicos pode ser expressa como:
Dados: vanádio Z = 23.
Dados: vanádio Z = 23.
Q1797130
Química
Para estudar o produto de solubilidade, uma solução
saturada de cloreto de sódio sem corpo de fundo foi
preparada e algumas afirmações foram feitas.
1) Ao adicionar mais íons Na+ em solução, ocorrerá a precipitação do NaCl. 2) Com a adição de água na solução, a mesma manterá sua saturação. 3) O aumento na concentração de íons Na+ provoca um aumento no kps do NaCl.
Está(ão) correta(s) a(s) afirmativa(s):
1) Ao adicionar mais íons Na+ em solução, ocorrerá a precipitação do NaCl. 2) Com a adição de água na solução, a mesma manterá sua saturação. 3) O aumento na concentração de íons Na+ provoca um aumento no kps do NaCl.
Está(ão) correta(s) a(s) afirmativa(s):
Q1797131
Química
Na medicina veterinária, o cloreto de amônio (NH4Cl) é
utilizado como acidulante da urina com o objetivo de
evitar infecções. Para a produção do NH4Cl, é
empregada a reação do ácido clorídrico (HCl) com
amônia (NH3), representada abaixo:
HCl(aq) + NH3(aq) → NH4Cl(s)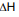 = ???
= ???
A partir dos valores das entalpias de formação do HCl ( = -46 kJ.mol-1), NH3 (
= -46 kJ.mol-1), NH3 ( = -92 kJ.mol-1) e NH4Cl (
= -92 kJ.mol-1) e NH4Cl ( = -314 kJ.mol-1), determine a variação de entalpia
(
= -314 kJ.mol-1), determine a variação de entalpia
(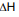 ) da reação acima e se o processo é endotérmico
ou exotérmico.
) da reação acima e se o processo é endotérmico
ou exotérmico.
HCl(aq) + NH3(aq) → NH4Cl(s)
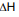 = ???
= ??? A partir dos valores das entalpias de formação do HCl (
 = -46 kJ.mol-1), NH3 (
= -46 kJ.mol-1), NH3 ( = -92 kJ.mol-1) e NH4Cl (
= -92 kJ.mol-1) e NH4Cl ( = -314 kJ.mol-1), determine a variação de entalpia
(
= -314 kJ.mol-1), determine a variação de entalpia
(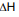 ) da reação acima e se o processo é endotérmico
ou exotérmico.
) da reação acima e se o processo é endotérmico
ou exotérmico.
Q1797132
Química
O carbono é encontrado na natureza em diferentes
arranjos e estruturas. O carbono diamante (Cdiam),
possui alto valor agregado e é formado sob alta
pressão, possuindo estrutura onde o carbono realiza
quatro ligações simples. Já o carbono grafite (Cgraf)
possui valor agregado muito baixo, comparado ao seu
alótropo diamante e realiza ligações duplas
conjugadas. As representações das estruturas dos
átomos de carbono nos diferentes alótropos, diamante
e grafite, estão representadas abaixo.
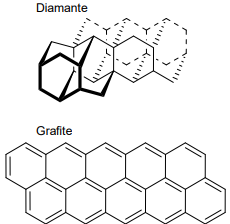
A partir das estruturas citadas e do enunciado da questão, podemos afirmar que a hibridização dos átomos de carbono presentes no diamante e no grafite são, respectivamente:

A partir das estruturas citadas e do enunciado da questão, podemos afirmar que a hibridização dos átomos de carbono presentes no diamante e no grafite são, respectivamente:
Q1797133
Química
Devido à alta dureza e ao elevado valor agregado do
carbono diamante (Cdiam), a conversão do carbono
grafite (Cgraf) em carbono diamante é algo viável em
termos comerciais, a partir da aplicação de alta
temperatura e pressão. Desta forma, o cálculo da
entalpia de reação para essa transformação pode ser
realizado a partir das reações de formação do gás
carbônico a partir do Cgraf e do Cdiam, expressas abaixo:
Cgraf + O2(g) → CO2(g) = -393,3 kJ Cdiam + O2(g) → CO2(g)
= -393,3 kJ Cdiam + O2(g) → CO2(g)  = -395,2 kJ Cgraf → Cdiam
= -395,2 kJ Cgraf → Cdiam  = ?
= ?
A partir dos valores de entalpia de formação do CO2, qual é a entalpia de reação para a transformação do carbono grafite em carbono diamante?
Cgraf + O2(g) → CO2(g)
 = -393,3 kJ Cdiam + O2(g) → CO2(g)
= -393,3 kJ Cdiam + O2(g) → CO2(g)  = -395,2 kJ Cgraf → Cdiam
= -395,2 kJ Cgraf → Cdiam  = ?
= ? A partir dos valores de entalpia de formação do CO2, qual é a entalpia de reação para a transformação do carbono grafite em carbono diamante?