Questões de Vestibular CESMAC 2015 para Prova Medicina-2016.1- 2° DIA- PROVA TIPO 1
Foram encontradas 2 questões
2 CrO42-(aq) + H+(aq)
 Cr2O72-(aq) + H2O(l)
Cr2O72-(aq) + H2O(l)
À partir deste equilíbrio, foram feitas três afirmações:
1) Em pH ácido, o equilíbrio será deslocado para a formação do íon dicromato.
2) Em pH básico, o equilíbrio será deslocado para a formação de íon cromato.
3) O equilíbrio químico não é dinâmico, por isso acima de pH 7 deve ocorrer o consumo total de íons dicromato.
Está(ão) correta(s) a(s) afirmativa(s):
H2(g) + S(s)
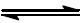 H2S(g)
H2S(g)
as quantidades de gás hidrogênio e sulfeto de hidrogênio são 0,40 g e 0,47 g, respectivamente, determine a constante de equilíbrio, Kc para a reação em estudo.
Dados: Massas molares em g . mol−1 : H = 1; S = 32.