Questões de Vestibular CEDERJ 2013 para Vestibular
Foi encontrada 1 questão
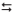 NH4(aq) + OH−
(aq) , assinale a alternativa que
apresenta a concentração do íon OH−
em mol/L e o pH da
solução nas condições dadas. Considere que para o
hidróxido de amônio Kb=1,0x10-5.
NH4(aq) + OH−
(aq) , assinale a alternativa que
apresenta a concentração do íon OH−
em mol/L e o pH da
solução nas condições dadas. Considere que para o
hidróxido de amônio Kb=1,0x10-5.