Questões de Vestibular de Química - Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão.
Foram encontradas 75 questões

Um aluno do curso de química em uma aula prática de Química Geral, precisa preparar uma solução de hidróxido de potássio de pH = 12 a 25ºC. qual a massa de KOH que ele precisa dissolver em 200 mL de água para obter o pH desejado?
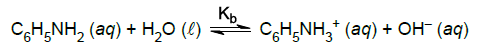
Sabe-se que Kb ≈ 4 × 10–10 a 25 ºC e que o valor de pH de uma solução aquosa saturada de anilina a 25 ºC é próximo de 9. Com base nessas informações e sabendo que Kw nessa temperatura é igual a 1 × 10–14, a concentração aproximada da solução saturada de anilina a 25 ºC é
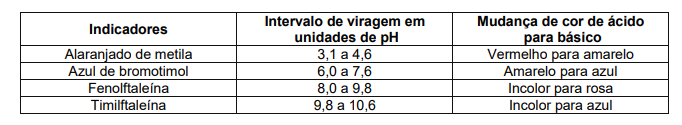
Uma amostra de água mineral natural a 25 °C foi testada com três indicadores ácido-base. Os resultados desse teste estão indicados na última coluna da tabela.

Analisando as informações da tabela e sabendo que o
produto iônico da água a 25 °C, Kw, é igual a 1 × 10−14, a
concentração de íons OH− (aq) nessa água mineral, em
mol/L, está entre

A esses frascos foi adicionado extrato de repolho roxo, um indicador ácido-base. Em meio muito ácido, esse extrato adquire coloração vermelha; em meio moderadamente ácido, rosa; e em meio básico, verde.
As colorações dos líquidos contidos nesses frascos, respectivamente, após a adição do extrato são:
Para diferenciar-se uma solução de pH=5,0 de uma solução de pH=8,0, ambas incolores, deve-se usar o indicador