Questões de Vestibular de Química - Representação das transformações químicas
Foram encontradas 193 questões
Ano: 2020
Banca:
COMVEST - UNICAMP
Órgão:
UNICAMP
Prova:
COMVEST - UNICAMP - 2020 - UNICAMP - Vestibular - Engenharia Química |
Q1697184
Química
Um determinado sólido contendo 20,0% em massa de
água necessita ser secado para produzir um sólido que
contenha no máximo 4,0% de água. A percentagem de
remoção de água do sólido original é igual a
Ano: 2020
Banca:
IMT - SP
Órgão:
IMT - SP
Prova:
IMT - SP - 2020 - IMT - SP - 2ª Aplicação - 01/12/2020 |
Q1692802
Química
O bicarbonato de sódio é empregado como
“fermento químico” em panificação, por sofrer a
seguinte reação de decomposição térmica não
balanceada: (Na = 23,0; H = 1,0; C = 12,0; O = 16,0 g/mol) 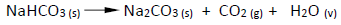
A termólise de 84 g do reagente produzirá a massa de carbonato de sódio e o número de mols de dióxido de carbono iguais a, respectivamente,
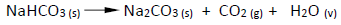
A termólise de 84 g do reagente produzirá a massa de carbonato de sódio e o número de mols de dióxido de carbono iguais a, respectivamente,
Ano: 2021
Banca:
UPENET/IAUPE
Órgão:
UPE
Prova:
UPENET/IAUPE - 2021 - UPE - Vestibular - 1º Fase - 2º Dia |
Q1680849
Química
Uma empresa faz diariamente entrega de produtos em Serra Talhada, sertão do Pajeú, a 420 km
de distância do Recife. O novo proprietário, preocupado com a imagem da empresa, realiza um teste
para considerar créditos de carbono. Segundo o computador de bordo, o rendimento médio do veículo
foi de 12 km por litro de combustível.
Considerando a composição da gasolina, essencialmente de moléculas com a fórmula C8H18 e
combustão completa de todo o combustível, qual o volume aproximado de gás carbônico (CO2), em
litros, liberado pelo veículo na viagem de ida e volta para entrega, em condições atmosféricas de
temperatura e pressão (CATP)?
Dados: Volume Molar (CATP) = 25 L; d(C8H18) = 800 g/L; Massas Molares – H = 1 g/mol; C = 12 g/mol; O = 16 g/mol
Dados: Volume Molar (CATP) = 25 L; d(C8H18) = 800 g/L; Massas Molares – H = 1 g/mol; C = 12 g/mol; O = 16 g/mol
Ano: 2021
Banca:
UPENET/IAUPE
Órgão:
UPE
Prova:
UPENET/IAUPE - 2021 - UPE - Vestibular - 1º Fase - 2º Dia |
Q1680845
Química
A reação química em que o alumínio é oxidado por um óxido de outro metal, geralmente óxido de
ferro, mediante alto aquecimento, é chamada termita, nome também dado à mistura entre os produtos
da reação. Considerando uma termita com 10,0 g de alumínio metálico (Al) e 100,0 g de óxido de ferro
III (Fe2O3), quantos gramas de ferro metálico são produzidos ao final do processo?
Al + Fe2O3 → Fe + Al2O3
Dados: Massas Molares – O = 16 g/mol; Al = 27 g/mol; Fe = 56 g/mol
Al + Fe2O3 → Fe + Al2O3
Dados: Massas Molares – O = 16 g/mol; Al = 27 g/mol; Fe = 56 g/mol
Ano: 2021
Banca:
CEV-URCA
Órgão:
URCA
Prova:
CEV-URCA - 2021 - URCA - Prova I - Física / Matemática / Química / Biologia |
Q1675980
Química

Segundo o site saúde.gov.br, diabetes é uma doença causada pela produção insuficiente ou má absorção de insulina, hormônio que regula a glicose no sangue e garante energia para o organismo. Para evitar que as células parem de funcionar, o organismo passa a usar os estoques de gordura para gerar energia. Só que nesse processo em que o corpo usa a gordura como energia, formam-se as cetonas. A equação química para a última etapa deste processo é a seguinte:
H3CCOCH2CO2H → H3CCOCH3 + CO2
A quantidade de acetona, produzida, em valores aproximados, que pode ser produzida a partir de 125 mg do ácido acetoacético, será: