Questões de Concurso
Comentadas para técnico de inspeção de equipamentos e instalações júnior
Foram encontradas 399 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A corrosão consiste na deterioração dos materiais pela ação química ou eletroquímica do meio e constitui uma reação indesejada de um material, a qual ocasiona sua dissolução ou o seu consumo, como a oxidação indesejada de um metal.
Os processos de fabricação atualmente apresentam grande importância tecnológica e sua racionalização promove a melhoria contínua das operações de qualidade. Julgue o item seguinte, referentes a processos de fabricação.
No processo de fabricação por usinagem, dá-se forma à peça
pela remoção progressiva de cavacos ou aparas de materiais
metálicos ou não, até serem atingidos a forma, a dimensão e
o tipo de acabamento desejados.
A soldagem é um dos mais importantes processos industriais de fabricação de peças metálicas. Considerando conceitos e campos de atuação da soldagem, julgue o item que se segue.
A soldagem é o processo de união de materiais, e a solda, o
resultado desse processo.
A soldagem é um dos mais importantes processos industriais de fabricação de peças metálicas. Considerando conceitos e campos de atuação da soldagem, julgue o item que se segue.
A soldagem a arco com eletrodos revestidos é um processo
de soldagem por fusão, no qual é utilizado o calor gerado
pelo arco formado entre o eletrodo de tungstênio não
consumível e a peça que se deseja soldar; nesse processo, o
arco elétrico produz energia térmica que impede a fusão
localizada do material de base e de adição.
A soldagem com eletrodo de tungstênio (TIG) é um processo no qual a união dos metais é obtida pelo seu aquecimento com um arco estabelecido entre um eletrodo especial consumível revestido e a peça que se deseja soldar; a alma desse eletrodo conduz a corrente elétrica e serve como metal de adição.
O petróleo é uma mistura complexa composta, em grande parte, por hidrocarbonetos. Julgue o próximo item, a respeito dos hidrocarbonetos.
Os hidrocarbonetos aromáticos, como o benzeno, são
compostos orgânicos em cuja estrutura há, pelo menos, um
anel benzênico.
Os hidrocarbonetos são compostos que consistem de apenas átomos de carbono e de oxigênio.
A estequiometria é aplicada em diversos estudos sobre a composição química de compostos e suas transformações químicas. No que se refere à estequiometria, julgue o item a seguir.
A estequiometria de uma reação apresenta a relação
qualitativa de reagentes formados e de produtos consumidos
nas diversas reações químicas indicadas por uma equação
química.
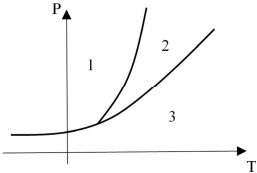
Na figura precedente, que corresponde ao diagrama de
fases de uma substância obtida a partir do fracionamento do
petróleo, as regiões 1, 2 e 3, delimitadas pelas curvas, estão
associadas aos estados físicos da substância, de acordo com as
condições de temperatura (T) e pressão (P).
Com base na figura e nas informações precedentes, julgue o próximo item.
A mudança de fase da substância do estado 1 diretamente
para o estado 3 corresponde ao que se denomina sublimação.
A respeito de transferência de calor, mudanças de estado e calorimetria, julgue o item que se segue.
Considere que a temperatura do petróleo extraído em uma
bacia terrestre seja igual a 110 °C. Nesse caso, se esse
petróleo for bombeado por meio de longas tubulações
metálicas até chegar aos tanques de armazenamento, o
petróleo não trocará calor com o meio externo.
A respeito de transferência de calor, mudanças de estado e calorimetria, julgue o item que se segue.
Se forem utilizadas tubulações de paredes duplas em um
processo de escoamento de petróleo no qual se produza
vácuo entre elas, haverá uma diminuição da transferência de
calor por condução e convecção entre o petróleo e o meio
externo.
Caso o petróleo extraído de um poço esteja armazenado em um tanque metálico por um tempo longo e suficiente para que esse petróleo esteja em equilíbrio térmico com as paredes do tanque e o meio externo, então, nessa situação, não haverá trocas de energia térmica entre o petróleo e o meio externo.
Um navio petroleiro transporta produtos derivados de petróleo, como diesel, nafta, gasolina, óleo combustível etc. Próximo a esse navio, foram colocadas boias esféricas de sinalização que flutuam parcialmente submersas.
Acerca dessa situação hipotética, e considerando que a massa de cada boia esférica seja igual a 2,0 kg, que a densidade da água seja igual a 103 kg/m3 e que a aceleração da gravidade seja igual a 10 m/s2 , julgue o item que se segue.
As boias flutuam parcialmente submersas porque são menos
densas que a água. Nesse sentido, é correto afirmar que
qualquer objeto flutuará se sua densidade for menor que a do
fluido em que ele estiver inserido.
A respeito das reações de oxirredução e dos ensaios não destrutivos, julgue o próximo item.
Quanto mais eletropositivo um elemento for, maior será sua
tendência de ganhar elétrons.
A respeito das reações de oxirredução e dos ensaios não destrutivos, julgue os próximos itens.
A inspeção visual, ensaio não destrutivo, envolve a
observação direta da superfície do material.
Os ensaios não destrutivos são técnicas utilizadas para avaliar a qualidade, a integridade e as características de componentes sem lhes causar danos permanentes ou destruição.
Acerca do diagrama de equilíbrio do aço-carbono, julgue o item que se segue.
No diagrama de equilíbrio do aço-carbono, em que são
representadas as fases e transformações que ocorrem em
ligas de ferro e carbono, o eixo vertical representa a
composição em porcentagem de carbono na liga, enquanto o
eixo horizontal representa a temperatura da liga.
Ao aumentar a temperatura de uma liga de ferro-carbono, a ferrita (α-ferro), de estrutura cúbica de corpo centrado, é transformada em austenita, de estrutura cúbica de face centrada.
Julgue o próximo item, referentes à medição de temperatura e suas escalas e à conversão de unidades.
A temperatura de 298 K equivale à temperatura de 78 °F.
Julgue o próximo item, referentes à medição de temperatura e suas escalas e à conversão de unidades.
A velocidade de 89 m/s equivale a uma velocidade superior a
315 km/h.