Questões de Concurso
Foram encontradas 1.417 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A entropia molar é uma medida da quantidade de desordem ou Incerteza em um sistema termodinâmico. É uma grandeza termodinâmica que mede a dispersão da energia e a quantidade de informação presente em um sistema. Para cada par apresentado, assinale a alternativa que apresenta as espécies com maior entropia molar a 298K:
I -HBr(g)e HF(g)
II- I2(s) el2(I)
III-Ar (g) a 1atm e Ar (g) a 2atm
Em relação às operações unitárias utilizadas em um laboratório de química, assinale a afirmativa correta.
O catalisador utilizado na oxidação da amônia está baseado em
Moléculas como água e amônia apresentam altas temperaturas de ebulição devido à (às)
Para um sistema fechado em repouso, isso se resume
dU = dQ + dW,
onde, U é energia interna; Q, calor, e W, trabalho. Outra função termodinâmica é a entalpia, H, que está corretamente definida na opção
Quando n = 1, o processo reversível em gases ideais é denominado
Assinale a opção que apresenta sua reação de decomposição com a estequiometria correta.
A mistura binária entre a água e o etanol forma
2 NO2 (g) + ½ O2 (g) + H2 O (g) ⇌ 2 HNO3 (g)
Considere que a reação foi simulada em laboratório, num reator com êmbolo, cujo volume e aquecimento podem ser variados.
É possível deslocar o equilíbrio para formar mais HNO3 , quando
Considere a Figura abaixo, que indica uma possível instalação para testes de escoamentos:
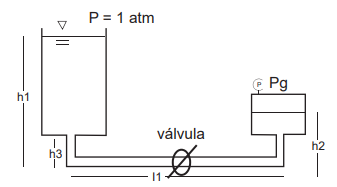
A válvula está fechada, e, nessa situação, não há escoamento. Pg é a pressão manométrica no ponto indicado do reservatório fechado da direita. A área da superfície livre do reservatório da esquerda é muito grande.
Sabendo-se que h1 = 7m; h2 = 1m; h3 = 4m e l1 = 100m;
g = 10 m/s2
e que a massa específica do fluido é igual a
1000 kg/m3
, Patm = 100 kPa, após a abertura da válvula, o
escoamento irá acontecer
Com essas informações, constata-se o seguinte:
Se a velocidade para M = 0,3 de um determinado gás (R = 300 J/kg.K) for igual a 106,5 m/s, a 27 ºC, a velocidade, em m/s, para a temperatura de 927 ºC será
Um trocador de calor opera nas condições abaixo:
Corrente quente:
cp = 4,5 kJ/kg.K
m ponto = 1,5 kg/s
t entrada = 200 ºC
t saída = 100 ºC
Corrente fria:
cp = 4,0 kJ/kg.K
Mponto = 2,5 kg/s
Tentrada = 15ºC
Tsaída = não informada
Qual é o valor da efetividade nas condições indicadas?
A temperatura desejada, em ºC, vale
Com base nessas informações, verifica-se o seguinte:
Esse valor para o coeficiente de fricção só é possível na seguinte circunstância:
Cx Hy + y (x + y/4) O2 → x CO2 + y/2 H2 O
Admita a composição molar do combustível Cx Hy em que a razão y/x = 2
Se for empregado O2 com 100% de excesso, então, a razão molar N2 /CO2 esperada na análise do gás de exaustão é, aproximadamente, de
Dado N2 /O2 no ar ≈ 3,7
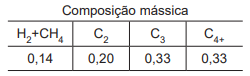
Considerando-se os resultados da análise, em base mássica, em relação ao gás que atravessa o gasoduto, conclui-se que