Questões da Prova FGV - 2016 - SEE-PE - Professor de Química
Foram encontradas 47 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A fórmula a seguir representa o ácido
7-[(1R,3R)-3-hidróxi-2-[(1E,3S)-3-hidróxi-oct-1-en-1-il] -5-oxo-ciclopentil]heptanoico,
foi uma das primeiras substâncias utilizadas para a impotência masculina. Os fármacos que possuíam esta droga na formulação deveriam ser injetados, o que tornava sua utilização inconveniente.
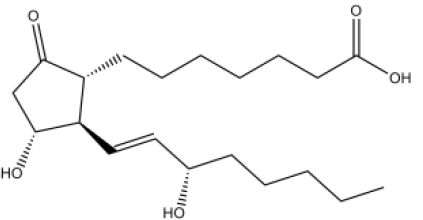
Analisando a nomenclatura e a fórmula desse ácido, é correto
afirmar que seus isômeros
Cientistas identificaram por meio de métodos cromatográficos que o extrato das folhas de lotus possui alcaloides com efeito psicotrópico. O extrato analisado foi administrado em cobaias e apresentou efeitos que superam os de ansiolíticos atualmente utilizados, com a vantagem de apresentar menos efeitos colaterais.
Entre os alcaloides identificados estão:
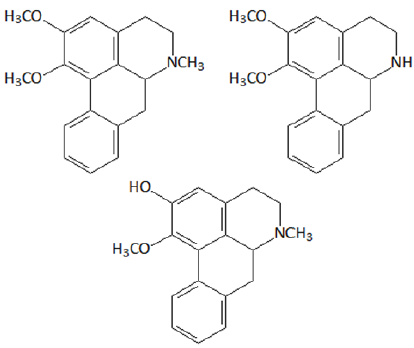
Assinale a opção que indica as funções orgânicas caracterizadas pelos grupos funcionais presentes nessas moléculas.
Nos atentados que ocorreram na cidade de Paris em 2015 os terroristas utilizaram o triperóxido de triacetona, o TATP, uma molécula altamente instável que pode ser detonada com facilidade e cuja está representada a seguir.
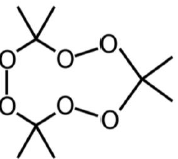
Esta molécula é obtida pela reação da acetona com água oxigenada e, portanto, não contém nitrogênio, tornando mais fácil a sua passagem por dispositivos de segurança que detectam compostos nitrogenados.
Na reação de síntese do TATP citada no enunciado, os carbonos
A análise da concentração de ortofosfato em corpos d’água pode ser feita utilizando o método colorimétrico. Nesse método, o reagente combinado contendo K(SbO)C4H4O6, (NH4)6Mo7O24 e ácido ascórbico reage em meio ácido com o ortofosfato, produzindo uma cor azul, cuja intensidade é determinada no espectrofotômetro.
No preparo de 100 mL do reagente combinado utiliza-se 5 mL de uma solução de K(SbO)C4H4O6 3,5 g.L-1 e 15 mL de uma solução de (NH4)6Mo7O24 40 g.L-1.
Nessa solução do reagente combinado as concentrações
aproximadas (em g.L-1 ) de K(SbO)C4H4O6 e de (NH4)6Mo7O24 são,
respectivamente,
Para quantificar sulfato em uma amostra adequadamente preparada foi elaborada uma curva de calibração a partir da diluição de uma solução padrão com concentração 100,0 mg.L-1 . A curva de calibração utilizou as seguintes soluções:
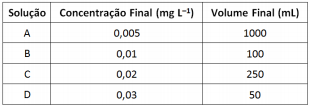
Sobre as soluções preparadas são feitas as afirmativas a seguir.
I. Para preparar as soluções A e C foram utilizados os mesmos volumes da solução padrão.Sobre as soluções preparadas são feitas as afirmativas a seguir.
II. Para preparar a solução B foi utilizado o menor volume da solução padrão.
III. Para preparar a solução D foi utilizado o maior volume da solução padrão.
Está correto o que se afirma em