Questões da Prova CESPE - 2013 - SEE-AL - Professor - Química
Foram encontradas 120 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!

A partir das informações contidas no fragmento de texto acima, julgue os itens que se seguem.
Considerando-se que o ar atmosférico que respiramos seja composto por CO2, O2, N2 e H2O, com 20,9% de O2, e que, no nível do mar, a pressão atmosférica seja de 760 mmHg, é correto afirmar que a pressão parcial exercida pelo O2 é de 0,209 atm.
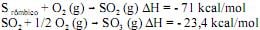
Considerando essas equações químicas, julgue os itens seguintes.
As reações de formação dos óxidos de enxofre são endotérmicas.
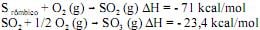
Considerando essas equações químicas, julgue os itens seguintes.
Para um processo que ocorre sob temperatura constante, a energia livre de Gibbs pode ser calculada por ΔG = ΔH - T ΔS.
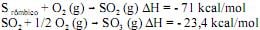
Considerando essas equações químicas, julgue os itens seguintes.
A entropia da reação global aumentou porque seu ΔH é mais negativo que os ΔH das etapas da reação.
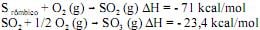
Considerando essas equações químicas, julgue os itens seguintes.
A reação global pode ser representada pela seguinte equação:
S rômbico + 3/2 O2 (g) → SO3 (g) ΔH = -94,4 kcal/mol.