Questões de Concurso Comentadas por alunos sobre balanço de massa e energia em engenharia química e química industrial
Foram encontradas 64 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2013
Banca:
CESPE / CEBRASPE
Órgão:
CPRM
Prova:
CESPE - 2013 - CPRM - Analista em Geociências - Química |
Q333994
Engenharia Química e Química Industrial
Texto associado
Julgue os itens a seguir, no que concerne aos balanços de massa e energia, que são fundamentais na definição global de um processo químico-industrial.
No balanço de energia em um processo exotérmico, o termo de geração associado ao calor gerado em processos reativos terá uma contribuição negativa para o processo.
Ano: 2012
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2012 - Transpetro - Químico de Petróleo Júnior |
Q258116
Engenharia Química e Química Industrial
Gás natural, cuja composição molar é 90% de metano, 7% de etano e 3% de propano, escoa no interior de uma tubulação de 0,05 m
2 de área de seção transversal, com velocidade uniforme igual a 0,28 m/s, na temperatura de 25 °C e pressão de 200 kPa.
Qual é a vazão mássica do gás natural nesse escoamento, expressa em kg/s, considerando comportamento ideal do gás. Dado constante universal dos gases R= 8,31 j/(mol-k)
Qual é a vazão mássica do gás natural nesse escoamento, expressa em kg/s, considerando comportamento ideal do gás. Dado constante universal dos gases R= 8,31 j/(mol-k)
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobrás - Engenheiro de Processamento Júnior |
Q188322
Engenharia Química e Química Industrial
Texto associado
Um mistura gasosa contendo  em proporções
em proporções
estequiométricas e na razão de 0,4 mol para 100 mol
na razão de 0,4 mol para 100 mol
de é carga fresca de um processo catalítico
é carga fresca de um processo catalítico
para a produção de metanol, de acordo com a equação:
 .
.
O efluente do reator passa por um processo de separação,
no qual todo o metanol e a água produzidos são separados
por condensação. Os gases contendo os reagentes não
reagidos e o são reciclados para o reator, misturando-
são reciclados para o reator, misturando-
-se com a carga fresca (F), dando origem à carga
combinada (CC). Para evitar acúmulo de no reator,
no reator,
parte da corrente gasosa é purgada, conforme o esquema
abaixo. A conversão global dos reagentes é de 96%. A
vazão molar de na carga fresca é de 5 mol/s.
na carga fresca é de 5 mol/s.

 em proporções
em proporções estequiométricas e
 na razão de 0,4 mol para 100 mol
na razão de 0,4 mol para 100 mol de
 é carga fresca de um processo catalítico
é carga fresca de um processo catalítico para a produção de metanol, de acordo com a equação:
 .
.O efluente do reator passa por um processo de separação,
no qual todo o metanol e a água produzidos são separados
por condensação. Os gases contendo os reagentes não
reagidos e o
 são reciclados para o reator, misturando-
são reciclados para o reator, misturando--se com a carga fresca (F), dando origem à carga
combinada (CC). Para evitar acúmulo de
 no reator,
no reator, parte da corrente gasosa é purgada, conforme o esquema
abaixo. A conversão global dos reagentes é de 96%. A
vazão molar de
 na carga fresca é de 5 mol/s.
na carga fresca é de 5 mol/s.
Considerando-se que a razão molar de reciclo (R/F), expressa apenas em termos de 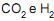 , é de 0,6, analise as afirmativas abaixo:
, é de 0,6, analise as afirmativas abaixo:
I - A conversão de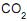 por passagem no reator é de 60%.
por passagem no reator é de 60%.
II - A vazão molar de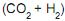 na carga combinada é 24 mol/s.
na carga combinada é 24 mol/s.
III - A razão molar de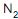 na corrente de carga combinada (CC) é de 0,10.
na corrente de carga combinada (CC) é de 0,10.
Está correto o que se afirma em
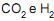 , é de 0,6, analise as afirmativas abaixo:
, é de 0,6, analise as afirmativas abaixo: I - A conversão de
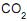 por passagem no reator é de 60%.
por passagem no reator é de 60%. II - A vazão molar de
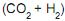 na carga combinada é 24 mol/s.
na carga combinada é 24 mol/s. III - A razão molar de
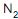 na corrente de carga combinada (CC) é de 0,10.
na corrente de carga combinada (CC) é de 0,10. Está correto o que se afirma em
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobrás - Engenheiro de Processamento Júnior |
Q188321
Engenharia Química e Química Industrial
Texto associado
Um mistura gasosa contendo  em proporções
em proporções
estequiométricas e na razão de 0,4 mol para 100 mol
na razão de 0,4 mol para 100 mol
de é carga fresca de um processo catalítico
é carga fresca de um processo catalítico
para a produção de metanol, de acordo com a equação:
 .
.
O efluente do reator passa por um processo de separação,
no qual todo o metanol e a água produzidos são separados
por condensação. Os gases contendo os reagentes não
reagidos e o são reciclados para o reator, misturando-
são reciclados para o reator, misturando-
-se com a carga fresca (F), dando origem à carga
combinada (CC). Para evitar acúmulo de no reator,
no reator,
parte da corrente gasosa é purgada, conforme o esquema
abaixo. A conversão global dos reagentes é de 96%. A
vazão molar de na carga fresca é de 5 mol/s.
na carga fresca é de 5 mol/s.

 em proporções
em proporções estequiométricas e
 na razão de 0,4 mol para 100 mol
na razão de 0,4 mol para 100 mol de
 é carga fresca de um processo catalítico
é carga fresca de um processo catalítico para a produção de metanol, de acordo com a equação:
 .
.O efluente do reator passa por um processo de separação,
no qual todo o metanol e a água produzidos são separados
por condensação. Os gases contendo os reagentes não
reagidos e o
 são reciclados para o reator, misturando-
são reciclados para o reator, misturando--se com a carga fresca (F), dando origem à carga
combinada (CC). Para evitar acúmulo de
 no reator,
no reator, parte da corrente gasosa é purgada, conforme o esquema
abaixo. A conversão global dos reagentes é de 96%. A
vazão molar de
 na carga fresca é de 5 mol/s.
na carga fresca é de 5 mol/s.
Com base nos dados acima, analise as afirmativas a seguir.
I - A vazão molar de metanol produzido é de 4,8 mol/s.
II - A fração molar de metanol na corrente de produto D é de 0,50.
III - A razão molar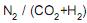 na corrente de purga P é de 0,10.
na corrente de purga P é de 0,10.
Está correto o que se afirma em
I - A vazão molar de metanol produzido é de 4,8 mol/s.
II - A fração molar de metanol na corrente de produto D é de 0,50.
III - A razão molar
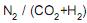 na corrente de purga P é de 0,10.
na corrente de purga P é de 0,10. Está correto o que se afirma em
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobrás - Engenheiro de Processamento Júnior |
Q188317
Engenharia Química e Química Industrial
Uma coluna de absorção foi dimensionada para absorver 90% de uma substância de massa molar igual a 50 kg/kmol, presente em uma corrente de ar, usando água pura como solvente. O teor dessa substância no ar é de 40% em base molar e, na solução aquosa formada, é de 25% em massa. Considerando-se que sejam desprezíveis a solubilidade do ar na água e a evaporação da água, a razão molar entre a água usada como solvente e a corrente de ar a ser tratada é
Dados: Massas molares: H = 1 kg/kmol; O = 16 kg/kmol; ar = 29 kg/kmol
Dados: Massas molares: H = 1 kg/kmol; O = 16 kg/kmol; ar = 29 kg/kmol