Questões de Concurso Sobre sistemas heterogêneos: produto de solubilidade (kps). em química
Foram encontradas 84 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Q1763748
Química
Em química analítica, é comum separar quantitativamente cátions através da precipitação fracionada
sob a forma de hidróxidos, bastando, para isso, fazer o controle adequado do pH do meio. Desse
modo, considere a separação de Mg2+ e Fe3+ a partir de uma solução 0,071 mol L-1 de Mg2+ e 2,0
mol L-1 de Fe3+. Sabendo-se que o produto de solubilidade do hidróxido de magnésio é 7,1x10-12 e o
produto de solubilidade do hidróxido de ferro é 2x10-39, o pH da solução para que o hidróxido mais
solúvel comece a precipitar é
Ano: 2021
Banca:
CESPE / CEBRASPE
Órgão:
Polícia Federal
Prova:
CESPE / CEBRASPE - 2021 - Polícia Federal - Papiloscopista Policial Federal |
Q1751775
Química
Uma das técnicas mais utilizadas para a coleta de impressões
digitais faz uso de pós. A interação dos pós com os componentes
da impressão digital se dá, normalmente, por interação de Van
der Waals. É comum utilizar óxido de ferro (III) — Fe2O3 — na
formulação desses pós. A revelação da impressão feita com
Fe2O3 pode ser destruída pela presença de ácido, por causa da
seguinte reação.
Fe2O3 (s) + x H+ (aq) ⇌ y Fe3+ (aq) + z H2O (l)
Com base nessas informações, julgue o seguinte item.
A constante de equilíbrio K da reação do óxido de ferro (III) é corretamente expressa pela seguinte equação. K = [ Fe3+ ]y [ H20]z / [Fe2O3] [ H+]x
Fe2O3 (s) + x H+ (aq) ⇌ y Fe3+ (aq) + z H2O (l)
Com base nessas informações, julgue o seguinte item.
A constante de equilíbrio K da reação do óxido de ferro (III) é corretamente expressa pela seguinte equação. K = [ Fe3+ ]y [ H20]z / [Fe2O3] [ H+]x
Q1396288
Química
Dada a reação de solubilidade que se
encontra em equilíbrio, assinale a alternativa
incorreta.
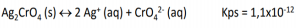
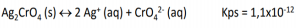
Q1396267
Química
Em relação a volumetria de precipitação,
assinale a alternativa incorreta.
Ano: 2019
Banca:
FUNDEP (Gestão de Concursos)
Órgão:
Prefeitura de Ervália - MG
Prova:
FUNDEP (Gestão de Concursos) - 2019 - Prefeitura de Ervália - MG - Professor - Química |
Q1311522
Química
Analise a situação a seguir.
Um químico recebeu uma amostra aquosa que continha,
entre outros solutos, 0,05 mol/L de íon magnésio e
0,01 mol/L de íon cálcio. A essa solução foi adicionado,
progressivamente, hidróxido de sódio sólido.
Supondo que não há mudança de volume com a adição do hidróxido de sódio e que a temperatura da solução, durante todo o processo reacional, permanece a 25 ºC, o químico chegou às seguintes conclusões:
I. O hidróxido de magnésio precipita primeiro que o hidróxido de cálcio. II. A concentração de íon magnésio que permanece na solução quando hidróxido de cálcio começa a precipitar é muito pequena. III. Não é necessário mais do que 0,06 mol/L de hidróxido de sódio para precipitar os dois íons na solução.
Dados: Kps (Mg(OH)2 ) = 1,1 x 10–11;
Kps (Ca(OH)2 ) = 5,5 x 10–6
Estão corretas as conclusões
Supondo que não há mudança de volume com a adição do hidróxido de sódio e que a temperatura da solução, durante todo o processo reacional, permanece a 25 ºC, o químico chegou às seguintes conclusões:
I. O hidróxido de magnésio precipita primeiro que o hidróxido de cálcio. II. A concentração de íon magnésio que permanece na solução quando hidróxido de cálcio começa a precipitar é muito pequena. III. Não é necessário mais do que 0,06 mol/L de hidróxido de sódio para precipitar os dois íons na solução.
Dados: Kps (Mg(OH)2 ) = 1,1 x 10–11;
Kps (Ca(OH)2 ) = 5,5 x 10–6
Estão corretas as conclusões