Questões da Prova CESGRANRIO - 2011 - Petrobras - Técnico Químico de Petróleo Júnior
Foram encontradas 40 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobras - Técnico Químico de Petróleo Júnior |
Q182900
Química
Texto associado
Considere o texto abaixo para responder às questões de nos 54 e 55.
O termo espectroscopia se refere ao estudo da interação da matéria com ondas eletromagnéticas ou, mais amplamente, com fontes de energia, incluindo, também, feixes de partículas como elétrons. O espectro eletromagnético abrange desde ondas de rádio (grandes comprimentos de
onda) até raios X (pequenos comprimentos de onda). entre esses extremos, há a radiação na região do infravermelho (IV), do visível e do ultravioleta (UV). A região da luz visível é uma pequena parte do espectro eletromagnético, que compreende radiações entre, aproximadamente,
400 e 700 nm.
As técnicas espectroscópicas desempenharam um papel central na descoberta de novos elementos e, também, na evolução do conhecimento sobre a estrutura do átomo,
como feito por Niels Bohr, ao estudar os espectros de absorção e emissão dos átomos.
O termo espectroscopia se refere ao estudo da interação da matéria com ondas eletromagnéticas ou, mais amplamente, com fontes de energia, incluindo, também, feixes de partículas como elétrons. O espectro eletromagnético abrange desde ondas de rádio (grandes comprimentos de
onda) até raios X (pequenos comprimentos de onda). entre esses extremos, há a radiação na região do infravermelho (IV), do visível e do ultravioleta (UV). A região da luz visível é uma pequena parte do espectro eletromagnético, que compreende radiações entre, aproximadamente,
400 e 700 nm.
As técnicas espectroscópicas desempenharam um papel central na descoberta de novos elementos e, também, na evolução do conhecimento sobre a estrutura do átomo,
como feito por Niels Bohr, ao estudar os espectros de absorção e emissão dos átomos.
O princípio da espectroscopia fotoeletrônica se baseia no efeito fotoelétrico, descoberto no final do século XIX por Heinrich Hertz. Nesse princípio, a incidência de luz na superfície de um metal levava à indução de corrente elétrica. Se um experimento semelhante é realizado no estado gasoso, pode-se medir a energia de ionização de um elemento: o fóton da luz incidente transfere energia para o elétron, que é ejetado. A diferença de energia do fóton e do elétron ejetado é a energia de ionização do elemento. Considere as afirmativas abaixo sobre esses experimentos.
I – A energia de cada fóton que incidirá na superfície metálica é independente da intensidade da luz.
II – Para que o efeito fotoelétrico seja observado no sódio, necessita-se de um maior comprimento de onda que o utilizado para o potássio.
III – O comprimento de onda necessário para que haja o efeito fotoelétrico aumentará com a dificuldade em ejetar os elétrons.
IV – Para um mesmo elemento, quanto menor o comprimento de onda da luz incidente, maior será a energia cinética do primeiro elétron ejetado.
Estão corretas APENAS as afirmativas
I – A energia de cada fóton que incidirá na superfície metálica é independente da intensidade da luz.
II – Para que o efeito fotoelétrico seja observado no sódio, necessita-se de um maior comprimento de onda que o utilizado para o potássio.
III – O comprimento de onda necessário para que haja o efeito fotoelétrico aumentará com a dificuldade em ejetar os elétrons.
IV – Para um mesmo elemento, quanto menor o comprimento de onda da luz incidente, maior será a energia cinética do primeiro elétron ejetado.
Estão corretas APENAS as afirmativas
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobras - Técnico Químico de Petróleo Júnior |
Q182899
Química
Texto associado
Considere o texto abaixo para responder às questões de nos 54 e 55.
O termo espectroscopia se refere ao estudo da interação da matéria com ondas eletromagnéticas ou, mais amplamente, com fontes de energia, incluindo, também, feixes de partículas como elétrons. O espectro eletromagnético abrange desde ondas de rádio (grandes comprimentos de
onda) até raios X (pequenos comprimentos de onda). entre esses extremos, há a radiação na região do infravermelho (IV), do visível e do ultravioleta (UV). A região da luz visível é uma pequena parte do espectro eletromagnético, que compreende radiações entre, aproximadamente,
400 e 700 nm.
As técnicas espectroscópicas desempenharam um papel central na descoberta de novos elementos e, também, na evolução do conhecimento sobre a estrutura do átomo,
como feito por Niels Bohr, ao estudar os espectros de absorção e emissão dos átomos.
O termo espectroscopia se refere ao estudo da interação da matéria com ondas eletromagnéticas ou, mais amplamente, com fontes de energia, incluindo, também, feixes de partículas como elétrons. O espectro eletromagnético abrange desde ondas de rádio (grandes comprimentos de
onda) até raios X (pequenos comprimentos de onda). entre esses extremos, há a radiação na região do infravermelho (IV), do visível e do ultravioleta (UV). A região da luz visível é uma pequena parte do espectro eletromagnético, que compreende radiações entre, aproximadamente,
400 e 700 nm.
As técnicas espectroscópicas desempenharam um papel central na descoberta de novos elementos e, também, na evolução do conhecimento sobre a estrutura do átomo,
como feito por Niels Bohr, ao estudar os espectros de absorção e emissão dos átomos.
Os espectros de absorção e emissão na região da luz visível para o átomo de hidrogênio foram estudos feitos por Balmer. Nessa região do espectro eletromagnético, ele observou um conjunto de quatro linhas: 656 nm, 486 nm, 434 nm e 410 nm.
Considerando-se que as transições eletrônicas observadas por Balmer no espectro de absorção partem do segundo nível energético do átomo de hidrogênio, a absorção da radiação de comprimento de onda de 656 nm leva o elétron ao
Considerando-se que as transições eletrônicas observadas por Balmer no espectro de absorção partem do segundo nível energético do átomo de hidrogênio, a absorção da radiação de comprimento de onda de 656 nm leva o elétron ao
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobras - Técnico Químico de Petróleo Júnior |
Q182898
Química
Deseja-se neutralizar 200 mL de uma solução aquosa 0,250 mol/L de ácido sulfúrico, utilizando-se 250 mL de uma solução de hidróxido de sódio. A concentração, em mol/L, dessa solução, e a massa, em gramas, de hidróxido de sódio necessária para prepará-la, são, respectivamente,
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobras - Técnico Químico de Petróleo Júnior |
Q182897
Química
Considere os seguintes potenciais padrão de eletrodo em meio ácido:
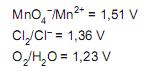
Nas condições padrão, haverá formação de gás pela reação entre
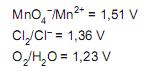
Nas condições padrão, haverá formação de gás pela reação entre
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Petrobras
Prova:
CESGRANRIO - 2011 - Petrobras - Técnico Químico de Petróleo Júnior |
Q182896
Química
A dispersão coloidal do tipo SOL é formada quando a fase dispersa e a fase de dispersão são, respectivamente,